Disciplina: Química 0 Curtidas
A partir de considerações teóricas, foi feita uma - FUVEST 2013
A partir de considerações teóricas, foi feita uma estimativa do poder calorífico (isto é, da quantidade de calor liberada na combustão completa de 1 kg de combustível) de grande número de hidrocarbonetos. Dessa maneira, foi obtido o seguinte gráfico de valores teóricos:
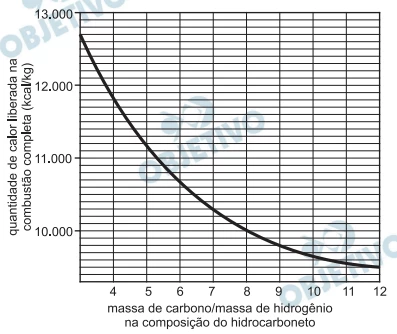
Com base no gráfico, um hidrocarboneto que libera 10.700 kcal/kg em sua combustão completa pode ser representado pela fórmula
Dados:
Massas molares (g/mol) C = 12,0
H = 1,00
-
CH4
-
C2H4
-
C4H10
-
C5H8
-
C6H6
Solução
Institução: FUVEST
Ano da Prova: 2013
Assuntos: Massas Molares
Vídeo Sugerido: YouTube
