Disciplina: Química 0 Curtidas
Analisando-se a equação de obtenção do estireno e - UNESP 2017
Leia o texto para responder às questões 74 e 75.
O estireno, matéria-prima indispensável para a produção do poliestireno, é obtido industrialmente pela desidrogenação catalítica do etilbenzeno, que se dá por meio do seguinte equilíbrio químico:
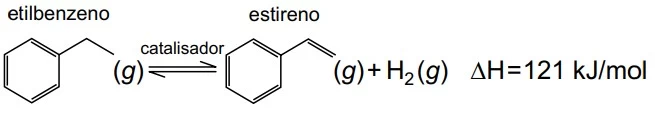
Analisando-se a equação de obtenção do estireno e considerando-se o princípio de Le Chatelier, é correto afirmar que
-
a entalpia da reação aumenta com o emprego do catalisador.
-
a entalpia da reação diminui com o emprego do catalisador.
-
o aumento de temperatura favorece a formação de estireno.
-
o aumento de pressão não interfere na formação de estireno.
-
o aumento de temperatura não interfere na formação de estireno.
Solução
Alternativa Correta: C) o aumento de temperatura favorece a formação de estireno.
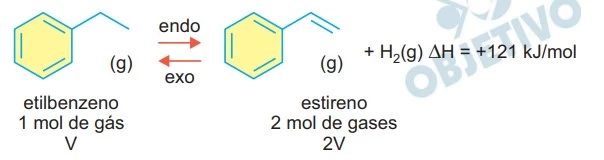
De acordo com o Princípio de Le Chatelier, o aumento de temperatura desloca o equilíbrio no sentido da reação endotérmica (formação do estireno). O aumento de pressão desloca o equilíbrio no sentido da contração de volume (formação do etilbenzeno). O catalisador diminui a energia de ativação, não alterando a entalpia da reação.
Resolução adaptada de: Curso Objetivo
Institução: UNESP
Ano da Prova: 2017
Assuntos: Princípio de Le Chatelier
Vídeo Sugerido: YouTube