Química
Exibindo questões de 101 a 200.
O volume de etanol, em litro, obtido nesse processo é mais - ENEM 2021
QuímicaA obtenção de etanol utilizando a cana-de-açúcar envolve a fermentação dos monossacarídeos formadores da sacarose contida no melaço. Um desses formadores é a glicose (C6H12O6), cuja fermentação produz cerca de 50 g de etanol a partir de 100 g de glicose, conforme a equação química descrita.
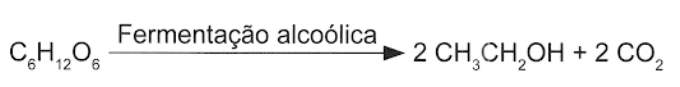
Em uma condição específica de fermentação, obtém-se 80% de conversão em etanol que, após sua purificação, apresenta densidade igual a 0,80 g/mL. O melaço utilizado apresentou 50 kg de monossacarídeos na forma de glicose.
O biocombustível a que se refere o texto é o - ENEM 2021
QuímicaCom o aumento da população de suínos no Brasil, torna-se necessária a adoção de métodos para reduzir o potencial poluidor dos resíduos dessa agroindústria, uma vez que, comparativamente ao esgoto doméstico, os dejetos suínos são 200 vezes mais poluentes. Sendo assim, a utilização desses resíduos como matéria-prima na obtenção de combustíveis é uma alternativa que permite diversificar a matriz energética nacional, ao mesmo tempo em que parte dos recursos hídricos do país são preservados.
As águas subterrâneas têm sido contaminadas pelo uso de - ENEM 2021
QuímicaAs águas subterrâneas têm sido contaminadas pelo uso de pesticidas na agricultura. Entre as várias substâncias usualmente encontradas, algumas são apresentadas na figura. A distinção dessas substâncias pode ser feita por meio de uma análise química quantitativa, ou seja, determinando sua presença mediante a adição de um reagente específico. O hidróxido de sódio é capaz de identificar a presença de um desses pesticidas pela reação ácido-base de Brönsted-Lowry.
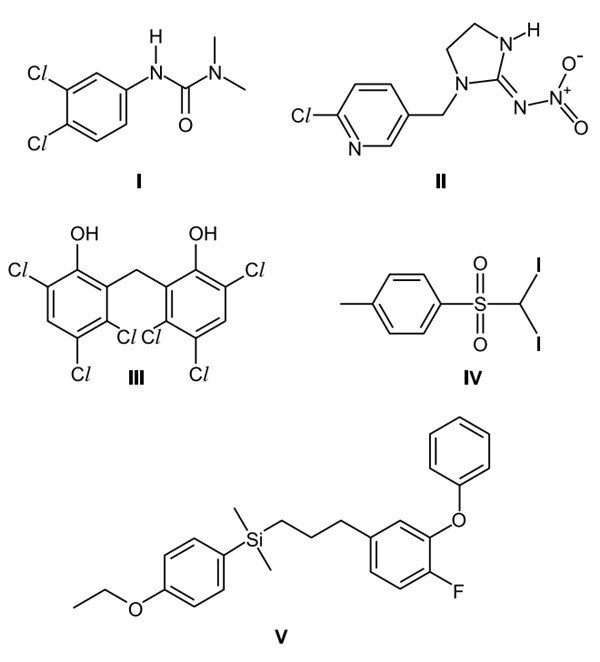
A tecnologia testada mais adequada para o emprego em - ENEM 2021
QuímicaO emprego de células de combustível a hidrogênio pode ser uma tecnologia adequada ao transporte automotivo. O quadro apresenta características de cinco tecnologias mais proeminentes de células de combustível.
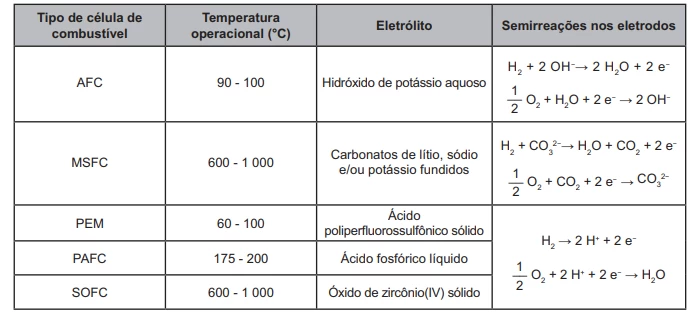
Testes operacionais com esses tipos de células têm indicado que as melhores alternativas para veículos são as que operam em baixos níveis de energia térmica, são formadas por membranas de eletrólitos poliméricos e ocorrem em meio ácido.
Na fototerapia, a luz provoca a conversão da bilirrubina - ENEM 2021
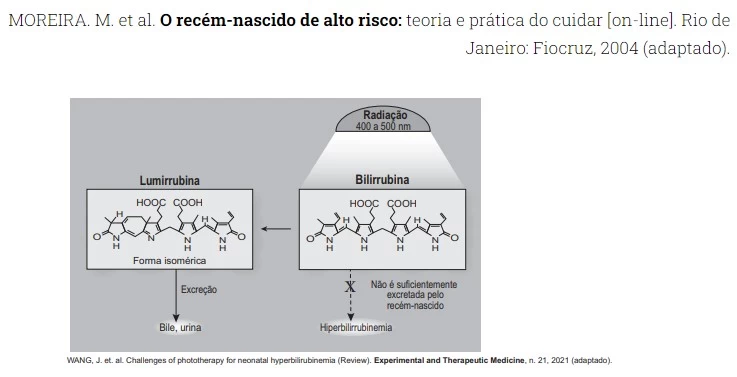
QuímicaA icterícia, popularmente conhecida por amarelão, é uma patologia frequente em recém-nascidos. Um bebê com icterícia não consegue metabolizar e excretar de forma eficiente a bilirrubina. Com isso, o acúmulo dessa substância deixa-o com a pele amarelada. A fototerapia é um tratamento de icterícia neonatal, que consiste na irradiação de luz no bebê. Na presença de luz, a bilirrubina é convertida no seu isômero lumirrubina que, por ser mais solúvel em água, é excretada pela bile ou pela urina. A imagem ilustra o que ocorre nesse tratamento.
Em qual etapa decanta-se o lodo a ser separado do esgoto - ENEM 2021
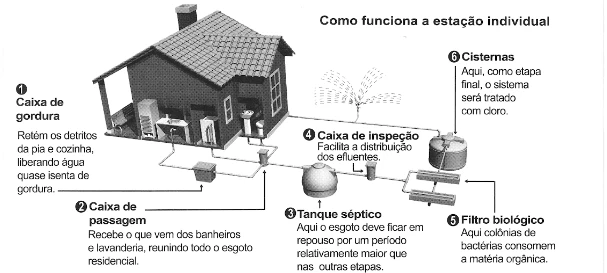
QuímicaA imagem apresenta as etapas do funcionamento de uma estação individual para tratamento do esgoto residencial.
O aroma do flavorizante derivado do ácido etanoico e que - ENEM 2021
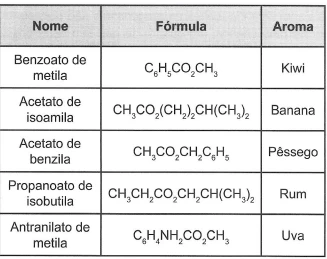
QuímicaCom o objetivo de proporcionar aroma e sabor a diversos alimentos, a indústria alimentícia se utiliza de flavorizantes. Em geral, essas substâncias são ésteres, como as apresentadas no quadro.
O Prêmio Nobel de Química de 2000 deveu-se à descoberta e - ENEM 2021
QuímicaO Prêmio Nobel de Química de 2000 deveu-se à descoberta e ao desenvolvimento de polímeros condutores. Esses materiais têm ampla aplicação em novos dispositivos eletroluminescentes (LEDs), células fotovoltaicas etc. Uma propriedade-chave de um polímero condutor é a presença de ligações duplas conjugadas ao longo da cadeia principal do polímero.
Essa bateria é adequada para o funcionamento de qual - ENEM 2021
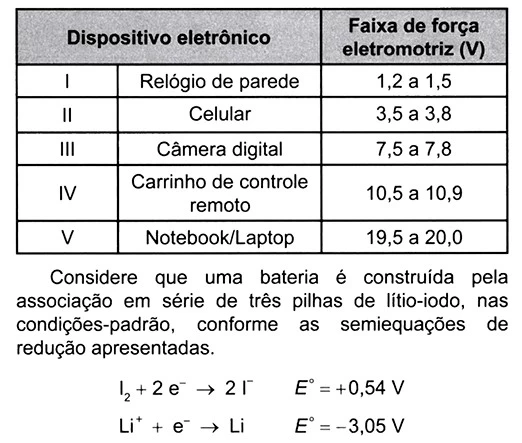
QuímicaO quadro lista alguns dispositivos eletrônicos que estão presentes no dia a dia, bem como a faixa de força eletromotriz necessária ao seu funcionamento.
Grande quantidade dos maus odores do nosso dia a dia está - ENEM 2014
QuímicaGrande quantidade dos maus odores do nosso dia a dia está relacionada a compostos alcalinos. Assim, em vários desses casos, pode-se utilizar o vinagre, que contém entre 3,5% e 5% de ácido acético, para diminuir ou eliminar o mau cheiro. Por exemplo, lavar as mãos com vinagre e depois enxaguá-las com água elimina o odor de peixe, já que a molécula de piridina (C5H5N) é uma das substâncias responsáveis pelo odor característico de peixe podre.
A liberação de gases clorofuorcarbonos (CFC) na atmosfera - ENEM 2014
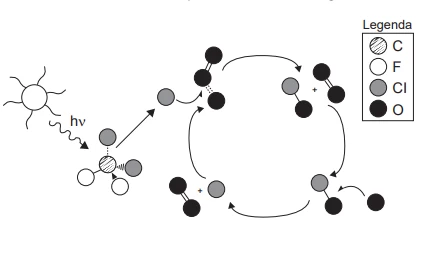
QuímicaA liberação de gases clorofuorcarbonos (CFC) na atmosfera pode provocar depleção de ozônio (O3) na estratosfera. O ozônio estratosférico é responsável por absorver parte da radiação ultravioleta emitida pelo Sol, a qual é nociva aos seres vivos. Esse processo, na camada de ozônio, é ilustrado simplificadamente na figura.
O biodiesel não é classificado como uma substância pura, - ENEM 2014
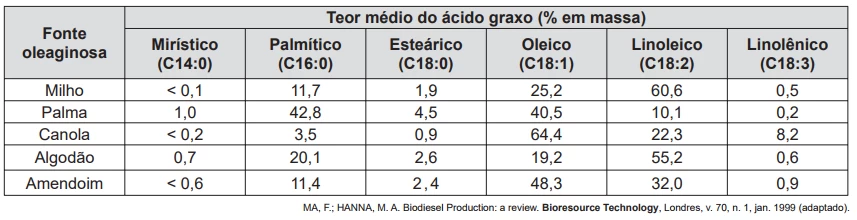
QuímicaO biodiesel não é classificado como uma substância pura, mas como uma mistura de ésteres derivados dos ácidos graxos presentes em sua matéria-prima. As propriedades do biodiesel variam com a composição do óleo vegetal ou gordura animal que lhe deu origem, por exemplo, o teor de ésteres saturados é responsável pela maior estabilidade do biodiesel frente à oxidação, o que resulta em aumento da vida útil do biocombustível. O quadro ilustra o teor médio de ácidos graxos de algumas fontes oleaginosas.
A talidomida é um sedativo leve e foi muito utilizado no - ENEM 2014
QuímicaA talidomida é um sedativo leve e foi muito utilizado no tratamento de náuseas, comuns no início da gravidez. Quando foi lançada, era considerada segura para o uso de grávidas, sendo administrada como uma mistura racêmica composta pelos seus dois enantiômeros (R e S). Entretanto, não se sabia, na época, que o enantiômero S leva à malformação congênita, afetando principalmente o desenvolvimento normal dos braços e pernas do bebê.
A utilização de processos de biorremediação de resíduos - ENEM 2014
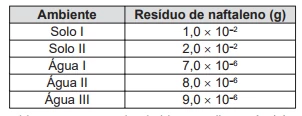
QuímicaA utilização de processos de biorremediação de resíduos gerados pela combustão incompleta de compostos orgânicos tem se tornado crescente, visando minimizar a poluição ambiental. Para a ocorrência de resíduos de naftaleno, algumas legislações limitam sua concentração em até 30 mg/kg para solo agrícola e 0,14 mg/L para água subterrânea. resíduo foi realizada em diferentes ambientes, utilizando-se amostras de 500 g de solo e 100 mL de água, conforme apresentado no quadro.
A revelação das chapas de raios X gera uma solução que - ENEM 2014
QuímicaA revelação das chapas de raios X gera uma solução que contém íons prata na forma de Ag(S2O3)2-3 . Para evitar a descarga desse metal no ambiente, a recuperação de prata metálica pode ser feita tratando eletroquimicamente essa solução com uma espécie adequada. O quadro apresenta semirreações de redução de alguns íons metálicos

A capacidade de limpeza e a eficiência de um sabão - ENEM 2014
QuímicaA capacidade de limpeza e a eficiência de um sabão dependem de sua propriedade de formar micelas estáveis, que arrastam com facilidade as moléculas impregnadas no material a ser limpo. Tais micelas têm em sua estrutura partes capazes de interagir com substâncias polares, como a água, e partes que podem interagir com substâncias apolares, como as gorduras e os óleos.
O principal processo industrial utilizado na produção de - ENEM 2014
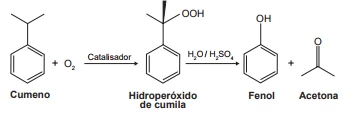
QuímicaO principal processo industrial utilizado na produção de fenol é a oxidação do cumeno (isopropilbenzeno). A equação mostra que esse processo envolve a formação do hidroperóxido de cumila, que em seguida é decomposto em fenol e acetona, ambos usados na indústria química como precursores de moléculas mais complexas. Após o processo de síntese, esses dois insumos devem ser separados para comercialização individual.
Diesel é uma mistura de hidrocarbonetos que também - ENEM 2014
QuímicaDiesel é uma mistura de hidrocarbonetos que também apresenta enxofre em sua composição. Esse enxofre é um componente indesejável, pois o trióxido de enxofre gerado é um dos grandes causadores da chuva ácida. Nos anos 1980, não havia regulamentação e era utilizado óleo diesel com 13 000 ppm de enxofre. Em 2009, o diesel passou a ter 1 800 ppm de enxofre (S1800) e, em seguida, foi inserido no mercado o diesel S500 (500 ppm). Em 2012, foi difundido o diesel S50, com 50 ppm de enxofre em sua composição. Atualmente, é produzido um diesel com teores de enxofre ainda menores.
Parte do gás carbônico da atmosfera é absorvida pela água - ENEM 2014
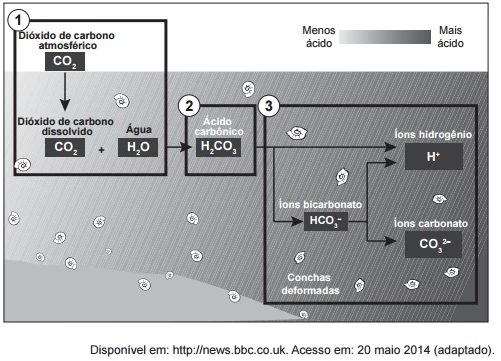
QuímicaParte do gás carbônico da atmosfera é absorvida pela água do mar. O esquema representa reações que ocorrem naturalmente, em equilíbrio, no sistema ambiental marinho. O excesso de dióxido de carbono na atmosfera pode afetar os recifes de corais.
Com o objetivo de substituir as sacolas de polietileno, - ENEM 2014
QuímicaCom o objetivo de substituir as sacolas de polietileno, alguns supermercados têm utilizado um novo tipo de plástico ecológico, que apresenta em sua composição amido de milho e uma resina polimérica termoplástica, obtida a partir de uma fonte petroquímica.
O estudo de compostos orgânicos permite aos analistas - ENEM 2014
QuímicaO estudo de compostos orgânicos permite aos analistas definir propriedades físicas e químicas responsáveis pelas características de cada substância descoberta. Um laboratório investiga moléculas quirais cuja cadeia carbônica seja insaturada, heterogênea e ramificada.
Grandes fontes de emissão do gás dióxido de enxofre são as - ENEM 2014
QuímicaGrandes fontes de emissão do gás dióxido de enxofre são as indústrias de extração de cobre e níquel, em decorrência da oxidação dos minérios sulfurados. Para evitar a liberação desses óxidos na atmosfera e a consequente formação da chuva ácida, o gás pode ser lavado, em um processo conhecido como dessulfurização, conforme mostrado na equação (1).
CaCO3(s) + SO2(g) → CaSO3(s) + CO2(g) (1)
Por sua vez, o sulfito de cálcio formado por ser oxidado, com o auxílio do ar atmosférico, para a obtenção do sulfato de cálcio, como mostrado na equação (2). Essa etapa é de grande interesse porque o produto da reação, popularmente conhecido como gesso, é utilizado para fins agrícolas.
2 CaSO3(s) + O2(g) → 2CaSO4(s) (2)
As massas molares dos elementos carbono, oxigênio, enxofre e cálcio são iguais a 12 g/mol, 16 g/mol, 32 g/mol e 40 g/mol, respectivamente.
A forma das moléculas, como representadas no papel, nem - ENEM 2014
QuímicaA forma das moléculas, como representadas no papel, nem sempre é planar. Em um determinado fármaco, a molécula contendo um grupo não planar é biologicamente ativa, enquanto moléculas contendo substituintes planares são inativas.
Visando minimizar impactos ambientais, a legislação - ENEM 2014
QuímicaVisando minimizar impactos ambientais, a legislação brasileira determina que resíduos químicos lançados diretamente no corpo receptor tenham pH entre 5,0 e 9,0. Um resíduo líquido aquoso gerado em um processo industrial tem concentração de íons hidroxila igual a 1,0 u 1010 mol/L. Para atender a legislação, um químico separou as seguintes substâncias, disponibilizadas no almoxarifado da empresa: CH3COOH, Na2SO4 , CH3 OH, K2CO3 e NH4Cl.
Para impedir a contaminação microbiana do suprimento de - ENEM 2014
QuímicaPara impedir a contaminação microbiana do suprimento de água, deve-se eliminar as emissões de efluentes e, quando necessário, tratá-lo com desinfetante. O ácido hipocloroso (HClO), produzido pela reação entre cloro e água, é um dos compostos mais empregados como desinfetante. Contudo, ele não atua somente como oxidante, mas também como um ativo agente de cloração. A presença de matéria orgânica dissolvida no suprimento de água clorada pode levar à formação de clorofórmio (CHCl3) e outras espécies orgânicas cloradas tóxicas.
A soda cáustica pode ser usada no desentupimento de - Enem 2015
QuímicaA soda cáustica pode ser usada no desentupimento de encanamentos domésticos e tem, em sua composição, o hidróxido de sódio como principal componente, além de algumas impurezas. A soda normalmente é comercializada na forma sólida, mas que apresenta aspecto “derretido” quando exposta ao ar por certo período.
Um grupo de pesquisadores desenvolveu um método simples - Enem 2015
QuímicaUm grupo de pesquisadores desenvolveu um método simples, barato e eficaz de remoção de petróleo contaminante na água, que utiliza um plástico produzido a partir do líquido da castanha-de-caju (LCC). A composição química do LCC é muito parecida com a do petróleo e suas moléculas, por suas características, interagem formando agregados com o petróleo. Para retirar os agregados da água, os pesquisadores misturam ao LCC nanopartículas magnéticas.
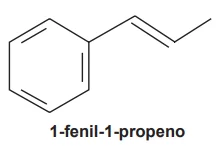
Os produtos obtidos na oxidação do alceno representado, em - Enem 2015
QuímicaO permanganato de potássio (KMnO4) é um agente oxidante forte muito empregado tanto em nível laboratorial quanto industrial. Na oxidação de alcenos de cadeia normal, como o 1-fenil-propeno, ilustrado na figura, o KMnO4 é utilizado para a produção de ácidos carboxílicos.
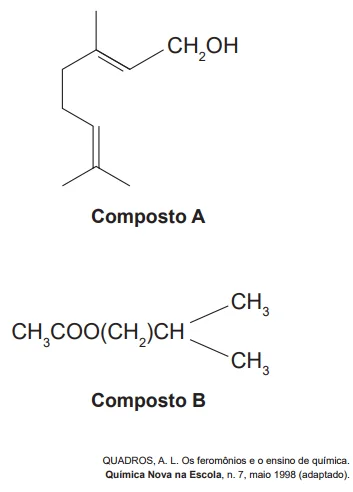
Uma forma de organização de um sistema biológico é a - Enem 2015
QuímicaUma forma de organização de um sistema biológico é a presença de sinais diversos utilizados pelos indivíduos para se comunicarem. No caso das abelhas da espécie Apis mellifera, os sinais utilizados podem ser feromônios. Para saírem e voltarem de suas colmeias, usam um feromônio que indica a trilha percorrida por elas (Composto A). Quando pressentem o perigo, expelem um feromônio de alarme (Composto B), que serve de sinal para um combate coletivo. O que diferencia cada um desses sinais utilizados pelas abelhas são as estruturas e funções orgânicas dos feromônios.
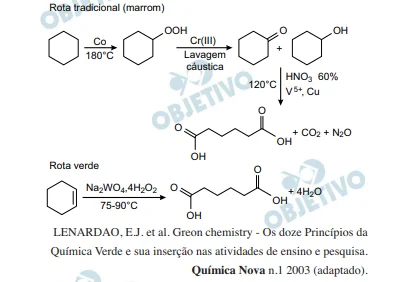
A química verde permite o desenvolvimento tecnológico com - Enem 2015
QuímicaA química verde permite o desenvolvimento tecnológico com danos reduzidos ao meio ambiente, e encontrar rotas limpas tem sido um grande desafio. Considere duas rotas diferentes utilizadas para a obtenção de ácido adípico, um insumo muito importante para a indústria têxtil e de lubrificantes
Alimentos em conserva são frequentemente armazenados em - Enem 2015
QuímicaAlimentos em conserva são frequentemente armazenados em latas metálicas seladas, fabricadas com um material chamado folha de flandres, que consiste de uma chapa de aço revestida com uma fina camada de estanho, metal brilhante e de difícil oxidação. É comum que a superfície interna seja ainda revestida por uma camada de verniz à base de epóxi, embora também existam latas sem esse revestimento, apresentando uma camada de estanho mais espessa.
A hidroponia pode ser definida como uma técnica de - Enem 2017
QuímicaA hidroponia pode ser definida como uma técnica de produção de vegetais sem necessariamente a presença de solo. Uma das formas de implementação é manter as plantas com suas raízes suspensas em meio líquido, de onde retiram os nutrientes essenciais. Suponha que um produtor de rúcula hidropônica precise ajustar a concentração do íon nitrato (NO3–) para 0,009 mol/L em um tanque de 5 000 litros e, para tanto, tem em mãos uma solução comercial nutritiva de nitrato de cálcio 90 g/L. As massas molares dos elementos N, O e Ca são iguais a 14 g/mol, 16 g/mol e 40 g/mol, respectivamente.
Pesticidas são substâncias utilizadas para promover o - Enem 2015
QuímicaPesticidas são substâncias utilizadas para promover o controle de pragas. No entanto, após sua aplicação em ambientes abertos, alguns pesticidas organoclorados são arrastados pela água até lagos e rios e, ao passar pelas guelras dos peixes, podem difundir-se para seus tecidos lipídicos e lá se acumularem.
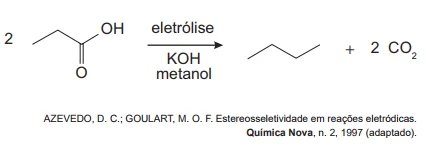
Hidrocarbonetos podem ser obtidos em laboratório por - Enem 2015
QuímicaHidrocarbonetos podem ser obtidos em laboratório por descarboxilação oxidativa anódica, processo conhecido como eletrossíntese de Kolbe. Essa reação é utilizada na síntese de hidrocarbonetos diversos, a partir de óleos vegetais, os quais podem ser empregados como fontes alternativas de energia, em substituição aos hidrocarbonetos fósseis. O esquema ilustra simplificadamente esse processo.
A calda bordalesa é uma alternativa empregada no combate - Enem 2015
QuímicaA calda bordalesa é uma alternativa empregada no combate a doenças que afetam folhas de plantas. Sua produção consiste na mistura de uma solução aquosa de sulfato de cobre(II), CuSO4, com óxido de cálcio, CaO, e sua aplicação só deve ser realizada se estiver levemente básica. A avaliação rudimentar da basicidade dessa solução é realizada pela adição de três gotas sobre uma faca de ferro limpa. Após três minutos, caso surja uma mancha avermelhada no local da aplicação, afirma-se que a calda bordalesa ainda não está com a basicidade necessária. O quadro apresenta os valores de potenciais padrão de redução (Eo) para algumas semirreações de redução.

Vários ácidos são utilizados em indústrias que descartam - Enem 2015
QuímicaVários ácidos são utilizados em indústrias que descartam seus efluentes nos corpos d’água, como rios e lagos, podendo afetar o equilíbrio ambiental. Para neutralizar a acidez, o sal carbonato de cálcio pode ser adicionado ao efluente, em quantidades apropriadas, pois produz bicarbonato, que neutraliza a água. As equações envolvidas no processo são apresentadas:
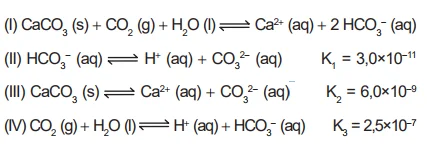
O aproveitamento de resíduos florestais vem se tornando - Enem 2015
QuímicaO aproveitamento de resíduos florestais vem se tornando cada dia mais atrativo, pois eles são uma fonte renovável de energia. A figura representa a queima de um bio-óleo extraído do resíduo de madeira, sendo ΔH1 a variação de entalpia devido à queima de 1g desse bio-óleo, resultando em gás carbônico e água líquida, e ΔH2 a variação de entalpia envolvida na conversão de 1g de água no estado gasoso para o estado líquido.
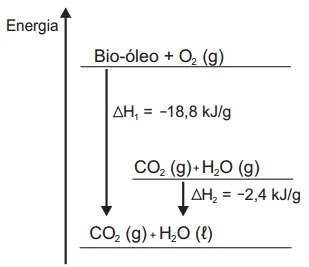
Para proteger estruturas de aço da corrosão, a indústria - Enem 2015
QuímicaPara proteger estruturas de aço da corrosão, a indústria utiliza uma técnica chamada galvanização. Um metal bastante utilizado nesse processo é o zinco, que pode ser obtido a partir de um minério denominado esfalerita (ZnS), de pureza 75%. Considere que a conversão do minério em zinco metálico tem rendimento de 80% nesta sequência de equações químicas:
2 ZnS + 3 O2 => 2 ZnO + 2 SO2
ZnO + CO => Zn + CO2
Considere as massas molares: ZnS (97 g/mol); O2 (32 g/mol); ZnO (81 g/mol); SO2 (64 g/mol); CO (28 g/mol); CO2 (44 g/mol); e Zn (65 g/mol).
Hipóxia ou mal das alturas consiste na diminuição de - Enem 2015
QuímicaHipóxia ou mal das alturas consiste na diminuição de oxigênio (O2) no sangue arterial do organismo. Por essa razão, muitos atletas apresentam mal-estar (dores de cabeça, tontura, falta de ar etc.) ao praticarem atividade física em altitudes elevadas. Nessas condições, ocorrerá uma diminuição na concentração de hemoglobina oxigenada (HbO2) em equilíbrio no sangue, conforme a relação:
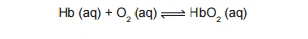
Uma pessoa abre sua geladeira, verifica o que há dentro - Enem 2015
QuímicaUma pessoa abre sua geladeira, verifica o que há dentro e depois fecha a porta dessa geladeira. Em seguida, ela tenta abrir a geladeira novamente, mas só consegue fazer isso depois de exercer uma força mais intensa do que a habitual.
Em um experimento, colocou-se água até a metade - Enem 2015
QuímicaEm um experimento, colocou-se água até a metade da capacidade de um frasco de vidro e, em seguida, adicionaram-se três gotas de solução alcoólica de fenolftaleína. Adicionou-se bicarbonato de sódio comercial, em pequenas quantidades, até que a solução se tornasse rosa. Dentro do frasco, acendeu-se um palito de fósforo, o qual foi apagado assim que a cabeça terminou de queimar. Imediatamente, o frasco foi tampado. Em seguida, agitou-se o frasco tampado e observou-se o desaparecimento da cor rosa.
Supondo que seja necessário dar um título para essa figura - Enem 2009
Química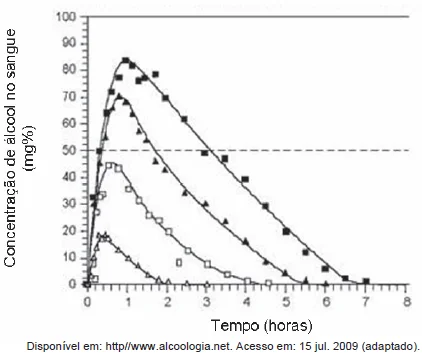
A Química Verde é um ramo da química que prega o - Enem 2020
QuímicaA Química Verde é um ramo da química que prega o desenvolvimento de processos eficientes, que transformem a maior parte do reagente em produto, de forma mais rápida e seletiva, que utilizem poucos reagentes, que produzam somente o produto desejado, evitando a formação de coprodutos, e que utilizem solventes não agressivos ao meio ambiente. Assim, as indústrias contornariam problemas relacionados à poluição ambiental e ao desperdício de água e energia.
Grandes reservatórios de óleo leve de melhor qualidade - Enem 2020
QuímicaGrandes reservatórios de óleo leve de melhor qualidade e que produz petróleo mais fino foram descobertos no litoral brasileiro numa camada denominada pré-sal, formada há 150 milhões de anos.
A sacarase (ou invertase) é uma enzima que atua no intestino-Enem 2020
QuímicaA sacarase (ou invertase) é uma enzima que atua no intestino humano hidrolisando o dissacarídeo sacarose nos monossacarídeos glicose e frutose. Em um estudo cinético da reação de hidrólise da sacarose (C12H22O11), foram dissolvidos 171 g de sacarose em 500 mL de água. Observou-se que, a cada 100 minutos de reação, a concentração de sacarose foi reduzida à metade, qualquer que fosse o momento escolhido como tempo inicial. As massas molares dos elementos H, C e O são iguais a 1, 12 e 16 g mo1–1, respectivamente.
A enorme quantidade de resíduos gerados pelo consumo - Enem 2020
QuímicaA enorme quantidade de resíduos gerados pelo consumo crescente da sociedade traz para a humanidade uma preocupação socioambiental, em especial pela quantidade de lixo produzido. Além da reciclagem e do reúso, pode-se melhorar ainda mais a qualidade de vida, substituindo polímeros convencionais por polímeros biodegradáveis.
Nos dias atuais, o amplo uso de objetos de plástico gera - Enem 2020
QuímicaNos dias atuais, o amplo uso de objetos de plástico gera bastante lixo, que muitas vezes é eliminado pela população por meio da queima. Esse procedimento é prejudicial ao meio ambiente por lançar substâncias poluentes. Para constatar esse problema, um estudante analisou a decomposição térmica do policloreto de vinila (PVC), um tipo de plástico, cuja estrutura é representada na figura.

Em 2011, uma falha no processo de perfuração realizado por - Enem 2020
QuímicaEm 2011, uma falha no processo de perfuração realizado por uma empresa petrolífera ocasionou derramamento de petróleo na bacia hidrográfica de Campos, no Rio de Janeiro.
Em seu laboratório, um técnico em química foi incumbido - Enem 2020
QuímicaEm seu laboratório, um técnico em química foi incumbido de tratar um resíduo, evitando seu descarte direto no meio ambiente. Ao encontrar o frasco, observou a seguinte informação: “Resíduo: mistura de acetato de etila e água”.
Considere os dados do acetato de etila:
• Baixa solubilidade em água; • Massa específica = 0,9 g cm–3;
• Temperatura de fusão = – 83°C;
• Pressão de vapor maior que a da água.
O crescimento da frota de veículos em circulação no mundo - Enem 2020
QuímicaO crescimento da frota de veículos em circulação no mundo tem levado à busca e desenvolvimento de tecnologias que permitam minimizar emissões de poluentes atmosféricos. O uso de veículos elétricos é uma das propostas mais propagandeadas por serem de emissão zero. Podemos comparar a emissão de carbono na forma de CO2 (massa molar igual a 44 g mol–1) para os dois tipos de carros (a combustão e elétrico). Considere que os veículos tradicionais a combustão, movidos a etanol (massa molar igual a 46 g mol–1), emitem uma média de 2,6 mol de CO2 por quilômetro rodado, e os elétricos emitem o equivalente a 0,45 mol de CO2 por quilômetro rodado (considerando as emissões na geração e transmissão da eletricidade). A reação e combustão do etanol pode ser representada pela equação química:
C2H5OH (l) + 3 O2 (g) → 2 CO2 (g) + 3 H2O (g)
Foram analisadas as emissões de CO2 envolvidas em dois veículos, um movido a etanol e outro elétrico, em um mesmo trajeto de 1 000 km.
As moedas despertam o interesse de colecionadores - Enem 2020
QuímicaAs moedas despertam o interesse de colecionadores, numismatas e investidores há bastante tempo. Uma moeda de 100% cobre, circulante no período do Brasil Colônia, pode ser bastante valiosa. O elevado valor gera a necessidade de realização de testes que validem a procedência da moeda, bem como a veracidade de sua composição. Sabendo que a densidade do cobre metálico é próxima de 9 g cm–3, um investidor negocia a aquisição de um lote de quatro moedas A, B, C e D fabricadas supostamente de 100% cobre e massas 26 g, 27 g, 10g e 36 g, respectivamente. Com o objetivo de testar a densidade das moedas, foi realizado um procedimento em que elas foram sequencialmente inseridas em uma proveta contendo 5 mL de água, conforme esquematizado.

Megaespetáculos com queima de grande quantidade de - Enem 2020
QuímicaMegaespetáculos com queima de grande quantidade de fogos de artifício em festas de final de ano são muito comuns no Brasil. Após a queima, grande quantidade de material particulado permanece suspensa no ar. Entre os resíduos, encontram-se compostos de sódio, potássio, bário, cálcio, chumbo, antimônio, cromo, além de percloratos e gases, como os dióxidos de nitrogênio e enxofre.
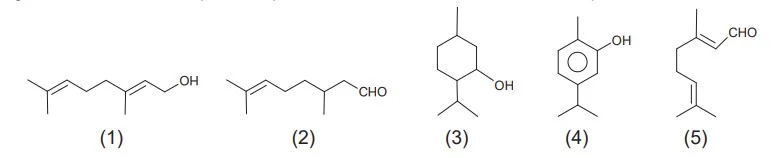
Um microempresário do ramo de cosméticos utiliza óleos - Enem 2020
QuímicaUm microempresário do ramo de cosméticos utiliza óleos essenciais e quer produzir um creme com fragrância de rosas. O principal componente do óleo de rosas tem cadeia poli-insaturada e hidroxila em carbono terminal. O catálogo dos óleos essenciais apresenta, para escolha da essência, estas estruturas químicas:
O dióxido de carbono passa para o estado sólido (gelo seco) -Enem 2020
QuímicaO dióxido de carbono passa para o estado sólido (gelo seco) a –78 °C e retorna ao estado gasoso à temperatura ambiente. O gás é facilmente solubilizado em água, capaz de absorver radiação infravermelha da superfície da terra e não conduz eletricidade. Ele é utilizado como matéria-prima para a fotossíntese até o limite de saturação. Após a fixação pelos organismos autotróficos, o gás retorna ao meio ambiente pela respiração aeróbica, fermentação, decomposição ou por resíduos industriais, queima de combustíveis fósseis e queimadas. Apesar da sua importância ecológica, seu excesso causa perturbações no equilíbrio ambiental.
A obtenção de óleos vegetais, de maneira geral, passa pelas -Enem 2020
QuímicaA obtenção de óleos vegetais, de maneira geral, passa pelas etapas descritas no quadro.

Embora a energia nuclear possa ser utilizada para fins - Enem 2020
QuímicaEmbora a energia nuclear possa ser utilizada para fins pacíficos, recentes conflitos geopolíticos têm trazido preocupações em várias partes do planeta e estimulado discussões visando o combate ao uso de armas de destruição em massa. Além do potencial destrutivo da bomba atômica, uma grande preocupação associada ao emprego desse artefato bélico é a poeira radioativa deixada após a bomba ser detonada.
Para garantir que produtos eletrônicos estejam armazenados - Enem 2020
QuímicaPara garantir que produtos eletrônicos estejam armazenados de forma adequada antes da venda, algumas empresas utilizam cartões indicadores de umidade nas embalagens desses produtos. Alguns desses cartões contêm um sal de cobalto que muda de cor em presença de água, de acordo com a equação química:
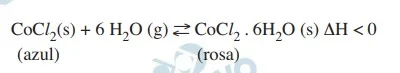
A nanotecnologia pode ser caracterizada quando os compostos -Enem 2020
QuímicaA nanotecnologia pode ser caracterizada quando os compostos estão na ordem de milionésimos de milímetros, como na utilização de nanomateriais catalíticos nos processos industriais. O uso desses materiais aumenta a eficiência da produção, consome menos energia e gera menores quantidades de resíduos. O sucesso dessa aplicação tecnológica muitas vezes está relacionado ao aumento da velocidade da reação química envolvida.
Na indústria farmacêutica, é muito comum o emprego de - Enem 2020
Química"Na indústria farmacêutica, é muito comum o emprego de substâncias de revestimento em medicamentos de uso oral, pois trazem uma série de benefícios como alteração de sabor em medicamentos que tenham gosto ruim, melhoria da assimilação do composto, entre outras ações. Alguns compostos poliméricos à base do polissacarídeo celulose são utilizados para garantir que o fármaco somente seja liberado quando em contato com soluções aquosas cujo pH se encontre próximo da faixa da neutralidade".
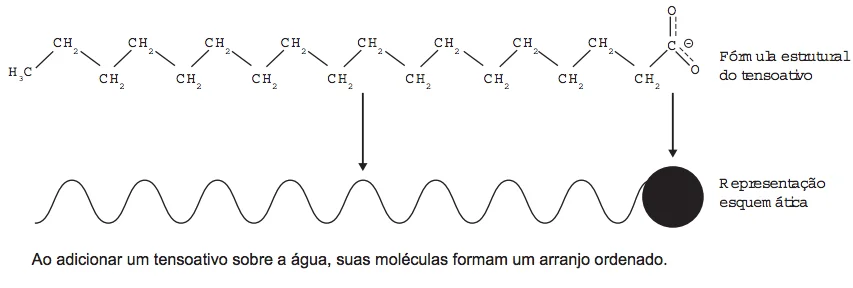
Os tensoativos são compostos capazes de interagir com - Enem 2016
QuímicaOs tensoativos são compostos capazes de interagir com substâncias polares e apolares. A parte iônica dos tensoativos interage com substâncias polares, e a parte lipofílica interage com as apolares. A estrutura orgânica de um tensoativo pode ser representada por:
Nucleófilos (Nu–) são bases de Lewis que reagem com haletos -Enem 2016
QuímicaNucleófilos (Nu–) são bases de Lewis que reagem com haletos de alquila, por meio de uma reação chamada substituição nucleofílica (SN), como mostrado no esquema:
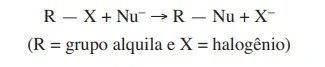
Pesquisadores recuperaram DNA de ossos de mamute - Enem 2016
QuímicaPesquisadores recuperaram DNA de ossos de mamute (Mammuthus primigenius) encontrados na Sibéria, que tiveram sua idade de cerca de 28 mil anos confirmada pela técnica do carbono-14.
Para cada litro de etanol produzido em uma indústria - Enem 2016
QuímicaPara cada litro de etanol produzido em uma indústria de cana-de-açúcar são gerados cerca de 18 L de vinhaça que é utilizada na irrigação das plantações de cana-de-açúcar, já que contém teores médios de nutrientes N, P e K iguais a 357 mg/L, 60 mg/L e 2 034 mg/L, respectivamente.
SILVA, M. A. S.; GRIEBELER, N. P.; BORGES, L. C. Uso de vinhaça e impactos nas propriedades do solo e lençol freático. Revista Brasileira de Engenharia Agrícola e Ambiental, n. 1, 2007 (adaptado).
Primeiro, em relação àquilo a que chamamos água - Enem 2016
QuímicaPrimeiro, em relação àquilo a que chamamos água, quando congela, parece-nos estar a olhar para algo que se tornou pedra ou terra, mas quando derrete e se dispersa, esta torna-se bafo e ar; o ar, quando é queimado, torna-se fogo; e, inversamente, o fogo, quando se contrai e se extingue, regressa à forma do ar; o ar, novamente concentrado e contraído, torna-se nuvem e nevoeiro, mas, a partir destes estados, se for ainda mais comprimido, torna-se água corrente, e de água torna-se novamente terra e pedras; e deste modo, como nos parece, dão geração uns aos outros de forma cíclica.
Biocélulas combustíveis são uma alternativa tecnológica - Enem 2016
QuímicaTEXTO I
Biocélulas combustíveis são uma alternativa tecnológica para substituição das baterias convencionais. Em uma biocélula microbiológica, bactérias catalisam reações de oxidação de substratos orgânicos. Liberam elétrons produzidos na respiração celular para um eletrodo, onde fluem por um circuito elétrico até o cátodo do sistema, produzindo corrente elétrica. Uma reação típica que ocorre em biocélulas microbiológicas utiliza o acetato como substrato.
AQUINO NETO, S. Preparação e caracterização de bioanodos para biocélula a combustível etanol/O2 . Disponível em: www.teses.usp.br. Acesso em: 23 jun. 2015 (adaptado).
TEXTO II
Em sistemas bioeletroquímicos, os potenciais padrão (E°’) apresentam valores característicos. Para as biocélulas de acetato, considere as seguintes semirreações de redução e seus respectivos potenciais:

A lipofilia é um dos fatores fundamentais para o - Enem 2016
QuímicaA lipofilia é um dos fatores fundamentais para o planejamento de um fármaco. Ela mede o grau de afinidade que a substância tem com ambientes apolares, podendo ser avaliada por seu coeficiente de partição.
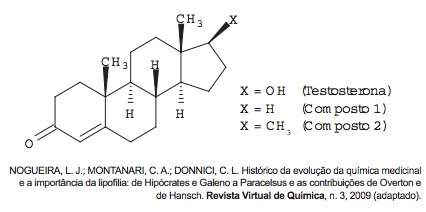
Após seu desgaste completo, os pneus podem ser queimados - Enem 2016
QuímicaApós seu desgaste completo, os pneus podem ser queimados para a geração de energia. Dentre os gases gerados na combustão completa da borracha vulcanizada, alguns são poluentes e provocam a chuva ácida. Para evitar que escapem para a atmosfera, esses gases podem ser borbulhados em uma solução aquosa contendo uma substância adequada. Considere as informações das substâncias listadas no quadro.
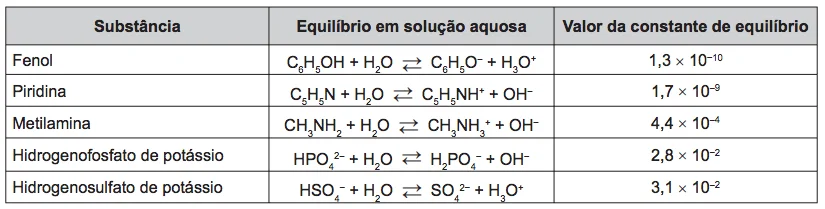
Os feromônios são substâncias utilizadas na comunicação - Enem 2016
QuímicaOs feromônios são substâncias utilizadas na comunicação entre indivíduos de uma espécie. O primeiro feromônio isolado de um inseto foi o bombicol, substância produzida pela mariposa do bicho-da-seda.
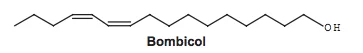
O uso de feromônios em ações de controle de insetos-praga está de acordo com o modelo preconizado para a agricultura do futuro. São agentes altamente específicos e seus compostos químicos podem ser empregados em determinados cultivos, conforme ilustrado no quadro.
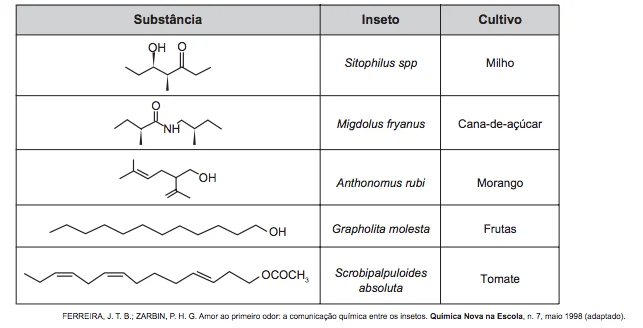
Em meados de 2003, mais de 20 pessoas morreram no Brasil - Enem 2016
QuímicaEm meados de 2003, mais de 20 pessoas morreram no Brasil após terem ingerido uma suspensão de sulfato de bário utilizada como contraste em exames radiológicos. O sulfato de bário é um sólido pouquíssimo solúvel em água, que não se dissolve mesmo na presença de ácidos. As mortes ocorreram porque um laboratório farmacêutico forneceu o produto contaminado com carbonato de bário, que é solúvel em meio ácido. Um simples teste para verificar a existência de íons bário solúveis poderia ter evitado a tragédia. Esse teste consiste em tratar a amostra com solução aquosa de HCl e, após filtrar para separar os compostos insolúveis de bário, adiciona-se solução aquosa de H2SO4 sobre o filtrado e observa-se por 30 minutos.
O aquecimento de um material por irradiação com - Enem 2016
QuímicaO aquecimento de um material por irradiação com micro-ondas ocorre por causa da interação da onda eletromagnética com o dipolo elétrico da molécula. Um importante atributo do aquecimento por micro-ondas é a absorção direta da energia pelo material a ser aquecido. Assim, esse aquecimento é seletivo e dependerá, principalmente, da constante dielétrica e da frequência de relaxação do material. O gráfico mostra a taxa de aquecimento de cinco solventes sob irradiação de micro-ondas.
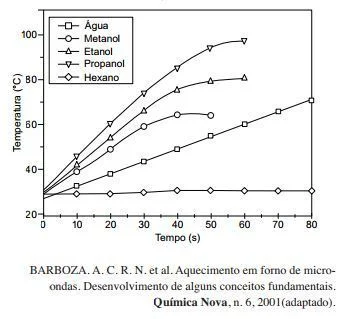
O carvão ativado é um material que possui elevado teor de - Enem 2016
QuímicaO carvão ativado é um material que possui elevado teor de carbono, sendo muito utilizado para a remoção de compostos orgânicos voláteis do meio, como o benzeno. Para a remoção desses compostos, utiliza-se a adsorção. Esse fenômeno ocorre por meio de interações do tipo intermoleculares entre a superfície do carvão (adsorvente) e o benzeno (adsorvato, substância adsorvida).
Em sua formulação, o spray de pimenta contém - Enem 2016
QuímicaEm sua formulação, o spray de pimenta contém porcentagens variadas de oleorresina de Capsicum, cujo princípio ativo é a capsaicina, e um solvente (um álcool como etanol ou isopropanol). Em contato com os olhos, pele ou vias respiratórias, a capsaicina causa um efeito inflamatório que gera uma sensação de dor e ardor, levando à cegueira temporária. O processo é desencadeado pela liberação de neuropeptídios das terminações nervosas.
A minimização do tempo e custo de uma reação química - Enem 2016
QuímicaA minimização do tempo e custo de uma reação química, bem como o aumento na sua taxa de conversão, caracterizam a eficiência de um processo químico. Como consequência, produtos podem chegar ao consumidor mais baratos. Um dos parâmetros que mede a eficiência de uma reação química é o seu rendimento molar (R, em %) definido como

em que n corresponde ao número de mols. O metanol pode ser obtido pela reação entre brometo de metila e hidróxido de sódio, conforme a equação química:
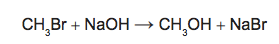
As massas molares (em g/mol) desses elementos são: H = 1; C = 12; O = 16; Na = 23; Br = 80.
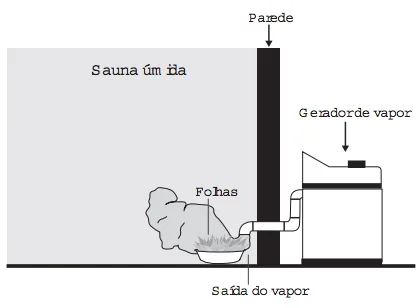
Uma pessoa é responsável pela manutenção de uma sauna - Enem 2016
QuímicaUma pessoa é responsável pela manutenção de uma sauna úmida. Todos os dias cumpre o mesmo ritual: colhe folhas de capim-cidreira e algumas folhas de eucalipto. Em seguida, coloca as folhas na saída do vapor da sauna, aromatizando-a, conforme mostrado na figura.
O benzeno, um importante solvente para a indústria química - Enem 2016
Química O benzeno, um importante solvente para a indústria química, é obtido industrialmente pela destilação do petróleo. Contudo, também pode ser sintetizado pela trimerização do acetileno catalisada por ferro metálico sob altas temperaturas, conforme a equação química:
3C2H2(g) → C6H6(l)
A energia envolvida nesse processo pode ser calculada indiretamente pela variação de entalpia das reações de combustão das substâncias participantes, nas mesmas condições experimentais:
I. C2H2(g) + 5/2O2(g) → 2CO2(g) + H2O(l) ∆Hco = –310 kcal/mol
II. C6H6(l) + 15/2O2(g) à 6CO2(g) + 3H2O(l) ∆Hco = –780 kcal/mol
A ozonólise, reação utilizada na indústria madeireira para - Enem 2017
QuímicaA ozonólise, reação utilizada na indústria madeireira para a produção de papel, é utilizada em escala de laboratório na síntese de aldeídos e cetonas. As duplas ligações dos alcenos são clivadas pela oxidação com o ozônio (O3), em presença de água e zinco metálico, e a reação produz aldeídos e/ou cetonas, dependendo do grau de substituição da ligação dupla. Ligações duplas dissubstituídas geram cetonas, enquanto as ligações duplas terminais ou monossubstituídas dão origem a aldeídos, como mostra o esquema.

Considere a ozonólise do composto 1-fenil-2-metilprop-1-eno:

A cromatografia em papel é um método de separação que - Enem 2017
QuímicaA cromatografia em papel é um método de separação que se baseia na migração diferencial dos componentes de uma mistura entre duas fases imiscíveis. Os componentes da amostra são separados entre a fase estacionária e a fase móvel em movimento no papel. A fase estacionária consiste de celulose praticamente pura, que pode absorver até 22% de água. É a água absorvida que funciona como fase estacionária líquida e que interage com a fase móvel, também líquida (partição líquido-líquido). Os componentes capazes de formar interações intermoleculares mais fortes com a fase estacionária migram mais lentamente.
Uma mistura de hexano com 5% (v/v) de acetona foi utilizada como fase móvel na separação dos componentes de um extrato vegetal obtido a partir de pimentões. Considere que esse extrato contém as substâncias representadas.

No ar que respiramos existem os chamados “gases inertes”. - Enem 2017
QuímicaNo ar que respiramos existem os chamados “gases inertes”. Trazem curiosos nomes gregos, que significam “o Novo”, “o Oculto”, “o Inativo”. E de fato são de tal modo inertes, tão satisfeitos em sua condição, que não interferem em nenhuma reação química, não se combinam com nenhum outro elemento e justamente por esse motivo ficaram sem ser observados durante séculos: só em 1962 um químico, depois de longos e engenhosos esforços, conseguiu forçar “o Estrangeiro” (o xenônio) a combinar-se fugazmente com o flúor ávido e vivaz, a façanha pareceu tão extraordinária que lhe foi conferido o Prêmio Nobel.
O ferro é encontrado na natureza na forma de seus minérios - Enem 2017
QuímicaO ferro é encontrado na natureza na forma de seus minérios, tais como a hematita (α-Fe2O3), a magnetita (Fe3O4) e a wustita (FeO). Na siderurgia, o ferro gusa é obtido pela fusão de minérios de ferro em altos fornos em condições adequadas. Uma das etapas nesse processo é a formação de monóxido de carbono. O CO (gasoso) é utilizado para reduzir o FeO (sólido), conforme a equação química:
FeO (s) + CO (g) –> Fe (s) + CO2 (g)
Considere as seguintes equações termoquímicas:
Fe2O3 (s) + 3 CO (g) –> 2 Fe (s) + 3 CO2 (g) ∆rH = –25 kJ/mol de Fe2O3
3 FeO (s) + CO2 (g) –> Fe3O4 (s) + CO (g) ∆rH = –36 kJ/mol de CO2
2 Fe3O4 (s) + CO2 (g) –> 3 Fe2O3 (s) + CO (g) ∆rH = +47 kJ/mol de CO2
O ácido acetilsalicílico, AAS massa molar igual a 180 g/mol -Enem 2017
QuímicaO ácido acetilsalicílico, AAS (massa molar igual a 180 g/mol), é sintetizado a partir da reação do ácido salicílico (massa molar igual a 138 g/mol) com anidrido acético, usando-se ácido sulfúrico como catalisador, conforme a equação química:

Após a síntese, o AAS é purificado e o rendimento flnal é de aproximadamente 50%. Devido às suas propriedades farmacológicas (antitérmico, analgésico, anti-inflamatório e antitrombótico), o AAS é utilizado como medicamento na forma de comprimidos, nos quais se emprega tipicamente uma massa de 500 mg dessa substância.
A invenção do LED azul, que permite a geração de outras - Enem 2017
QuímicaA invenção do LED azul, que permite a geração de outras cores para compor a luz branca, permitiu a construção de lâmpadas energeticamente mais eficientes e mais duráveis do que as incandescentes e fluorescentes. Em um experimento de laboratório, pretende-se associar duas pilhas em série para acender um LED azul que requer 3,6 volts para o seu funcionamento. Considere as semirreações de redução e seus respectivos potenciais mostrados no quadro.

Alguns tipos de dessalinizadores usam o processo de osmose - Enem 2017
QuímicaAlguns tipos de dessalinizadores usam o processo de osmose reversa para obtenção de água potável a partir da água salgada. Nesse método, utiliza-se um recipiente contendo dois compartimentos separados por uma membrana semipermeável: em um deles coloca-se água salgada e no outro recolhe-se a água potável. A aplicação de pressão mecânica no sistema faz a água fluir de um compartimento para o outro. O movimento das moléculas de água através da membrana é controlado pela pressão osmótica e pela pressão mecânica aplicada.
Diversos produtos naturais podem ser obtidos de plantas - Enem 2017
QuímicaDiversos produtos naturais podem ser obtidos de plantas por processo de extração. O lapachol é da classe das naftoquinonas. Sua estrutura apresenta uma hidroxila enólica (pKa = 6,0) que permite que este composto seja isolado da serragem dos ipês por extração com solução adequada, seguida de filtração simples. Considere que pKa = -log Ka, em que Ka é a constante ácida da reação de ionização do lapachol.

As centrífugas são equipamentos utilizados em laboratórios - Enem 2017
QuímicaAs centrífugas são equipamentos utilizados em laboratórios, clínicas e indústrias. Seu funcionamento faz uso da aceleração centrífuga obtida pela rotação de um recipiente e que serve para a separação de sólidos em suspensão em líquidos ou de líquidos misturados entre si.
O biodiesel é um biocombustível obtido a partir de fontes - Enem 2017
QuímicaO biodiesel é um biocombustível obtido a partir de fontes renováveis, que surgiu como alternativa ao uso do diesel de petróleo para motores de combustão interna. Ele pode ser obtido pela reação entre triglicerídeos, presentes em óleos vegetais e gorduras animais, entre outros, e álcoois de baixa massa molar, como o metanol ou etanol, na presença de um catalisador, de acordo com a equação química:
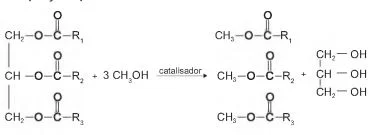
A farinha de linhaça dourada é um produto natural que - Enem 2017
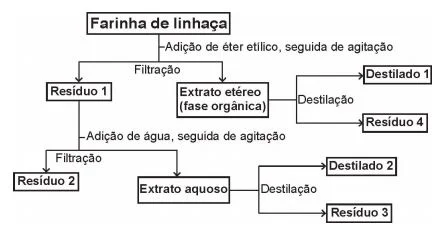
QuímicaA farinha de linhaça dourada é um produto natural que oferece grandes benefícios para o nosso organismo. A maior parte dos nutrientes da linhaça encontra-se no óleo desta semente, rico em substâncias lipossolúveis com massas moleculares elevadas. A farinha também apresenta altos teores de fibras proteicas insolúveis em água, celulose, vitaminas lipossolúveis e sais minerais hidrossolúveis.
Considere o esquema, que resume um processo de separação dos componentes principais da farinha de linhaça dourada.
Na Idade Média para elaborar preparados a partir de plantas -Enem 2017
QuímicaNa Idade Média, para elaborar preparados a partir de plantas produtoras de óleos essenciais, as coletas das espécies eram realizadas ao raiar do dia. Naquela época, essa prática era fundamentada misticamente pelo efeito mágico dos raios lunares, que seria anulado pela emissão dos raios solares. Com a evolução da ciência, foi comprovado que a coleta de algumas espécies ao raiar do dia garante a obtenção de material com maiores quantidades de óleos essenciais.
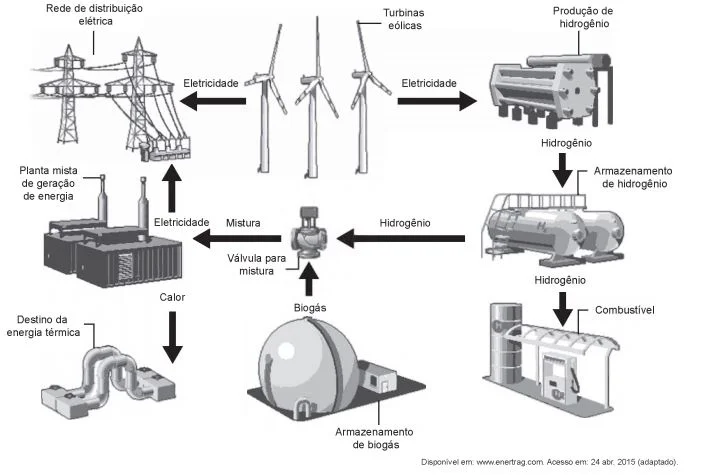
A figura mostra o funcionamento de uma estação híbrida - Enem 2017
QuímicaA figura mostra o funcionamento de uma estação híbrida de geração de eletricidade movida a energia eólica e biogás. Essa estação possibilita que a energia gerada no parque eólico seja armazenada na forma de gás hidrogênio, usado no fornecimento de energia para a rede elétrica comum e para abastecer células a combustível.
A técnica do carbono-14 permite a datação de fósseis - Enem 2017
QuímicaA técnica do carbono-14 permite a datação de fósseis pela medição dos valores de emissão beta desse isótopo presente no fóssil. Para um ser em vida, o máximo são 15 emissões beta/(min g). Após a morte, a quantidade de 14C se reduz pela metade a cada 5 730 anos.
Partículas microscópicas existentes na atmosfera funcionam - Enem 2017
QuímicaPartículas microscópicas existentes na atmosfera funcionam como núcleos de condensação de vapor de água que, sob condições adequadas de temperatura e pressão, propiciam a formação das nuvens e consequentemente das chuvas. No ar atmosférico, tais partículas são formadas pela reação de ácidos (HX) com a base NH3, de forma natural ou antropogênica, dando origem a sais de amônio (NH4X) , de acordo com a equação química genérica:
3(g) –> NH4X(s)
Um fato corriqueiro ao se cozinhar arroz é o derramamento - Enem 2017
QuímicaUm fato corriqueiro ao se cozinhar arroz é o derramamento de parte da água de cozimento sobre a chama azul do fogo, mudando-a para uma chama amarela. Essa mudança de cor pode suscitar interpretações diversas, relacionadas às substâncias presentes na água de cozimento. Além do sal de cozinha (NaCl), nela se encontram carboidratos, proteínas e sais minerais.
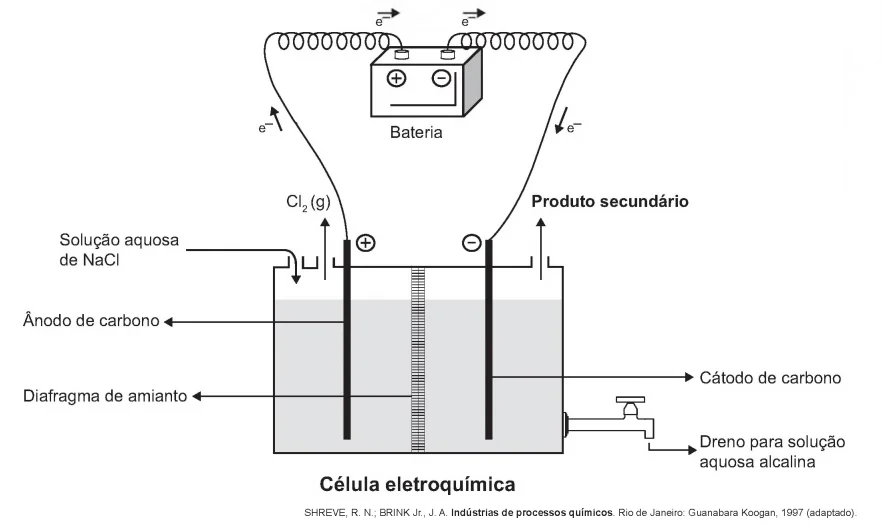
A eletrólise é um processo não espontâneo de grande - Enem 2017
QuímicaA eletrólise é um processo não espontâneo de grande importância para a indústria química. Uma de suas aplicações é a obtenção do gás cloro e do hidróxido de sódio, a partir de uma solução aquosa de cloreto de sódio. Nesse procedimento, utiliza-se uma célula eletroquímica, como ilustrado.
A toxicidade de algumas substâncias é normalmente - Enem 2017
QuímicaA toxicidade de algumas substâncias é normalmente representada por um índice conhecido como DL50 (dose letal mediana). Ele representa a dosagem aplicada a uma população de seres vivos que mata 50% desses indivíduos e é normalmente medido utilizando-se ratos como cobaias. Esse índice é muito importante para os seres humanos, pois ao se extrapolar os dados obtidos com o uso de cobaias, pode-se determinar o nível tolerável de contaminação de alimentos, para que possam ser consumidos de forma segura pelas pessoas. O quadro apresenta três pesticidas e suas toxicidades. A unidade mg/kg indica a massa da substância ingerida pela massa da cobaia.
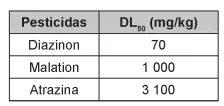
Sessenta ratos, com massa de 200 g cada, foram divididos em três grupos de vinte. Três amostras de ração, contaminadas, cada uma delas com um dos pesticidas indicados no quadro, na concentração de 3 mg por grama de ração, foram administradas para cada grupo de cobaias. Cada rato consumiu 100g de ração.
O petróleo é uma fonte de energia de baixo custo e de larga -Enem 2018
QuímicaO petróleo é uma fonte de energia de baixo custo e de larga utilização como matéria-prima para uma grande variedade de produtos. É um óleo formado de várias substâncias de origem orgânica, em sua maioria hidrocarbonetos de diferentes massas molares.
São utilizadas técnicas de separação para obtenção dos componentes comercializáveis do petróleo.
Além disso, para aumentar a quantidade de frações comercializáveis, otimizando o produto de origem fóssil, utiliza-se o processo de craqueamento.
As células e os organismos precisam realizar trabalho para - Enem 2018
QuímicaAs células e os organismos precisam realizar trabalho para permanecerem vivos e se reproduzirem. A energia metabólica necessária para a realização desse trabalho é oriunda da oxidação de combustíveis, gerados no ciclo do carbono, por meio de processos capazes de interconverter diferentes formas da energia.
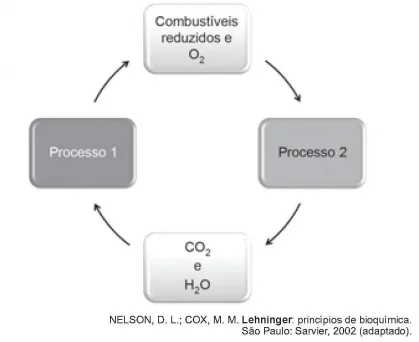
O manejo adequado do solo possibilita a manutenção de sua - Enem 2018
QuímicaO manejo adequado do solo possibilita a manutenção de sua fertilidade à medida que as trocas de nutrientes entre matéria orgânica, água, solo e o ar são mantidas para garantir a produção. Algumas espécies iônicas de alumínio são tóxicas, não só para a planta, mas para muitos organismos como as bactérias responsáveis pelas transformações no ciclo do nitrogênio. O alumínio danifica as membranas das células das raízes e restringe a expansão de suas paredes, com isso, a planta não cresce adequadamente. Para promover benefícios para a produção agrícola, é recomendada a remediação do solo utilizando calcário (CaCO3).
Tensoativos são compostos orgânicos que possuem - Enem 2018
QuímicaTensoativos são compostos orgânicos que possuem comportamento anfifílico. Isto é, possuem duas regiões, uma hidrofóbica e outra hidrofílica. O principal tensoativo aniônico sintético surgiu na década de 1940 e teve grande aceitação no mercado de detergentes em razão do melhor desempenho comparado ao do sabão. No entanto, o uso desse produto provocou grandes problemas ambientais, dentre eles a resistência ã degradação biológica, por causa dos diversos carbonos terciários na cadela que compõe a porção hidrofóbica desse tensoativo aniônico. As ramificações na cadela dificultam sua degradação, levando ã persistência no melo ambiente por longos períodos. Isso levou a sua substituição na maioria dos países por tensoativos biodegradáveis, ou seja, com cadeias alquílicas lineares.
Em 1938 o arqueólogo alemão WIlhelm Kõnlg, diretor do - Enem 2018
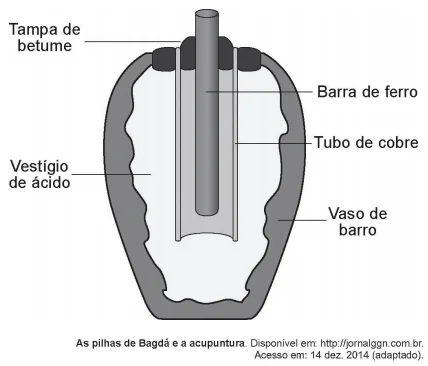
QuímicaEm 1938 o arqueólogo alemão Wilhelm König, diretor do Museu Nacional do Iraque, encontrou um objeto estranho na coleção da instituição, que poderia ter sido usado como uma pilha, similar às utilizadas em nossos dias. A suposta pilha, datada de cerca de 200 a.C., é constituída de um pequeno vaso de barro (argila) no qual foram instalados um tubo de cobre, uma barra de ferro (aparentemente corroída por ácido) e uma tampa de betume (asfalto), conforme ilustrado. Considere os potenciais-padrão de redução: E(Fe2+Fe) = –0,44 V; E(H+H2) = 0,00 V; e E(Cu2+Cu) = +0,34 V.
Alguns materiais sólidos são compostos por átomos que - Enem 2018
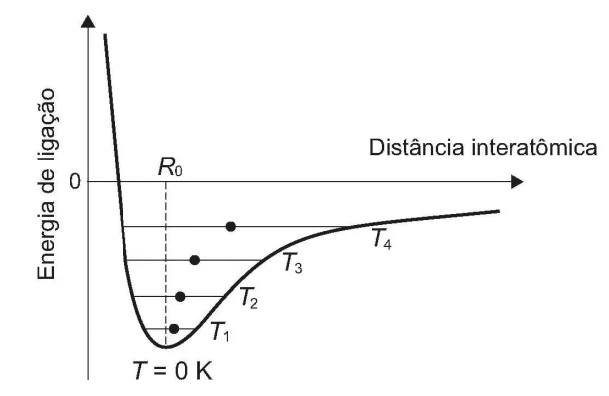
QuímicaAlguns materiais sólidos são compostos por átomos que interagem entre si formando ligações que podem ser covalentes, iônicas ou metálicas. A figura apresenta a energia potencial de ligação em função da distância interatômica em um sólido cristalino. Analisando essa figura, observa-se que, na temperatura de zero kelvin, a distância de equilíbrio da ligação entre os átomos (R0) corresponde ao valor mínimo de energia potencial. Acima dessa temperatura, a energia térmica fornecida aos átomos aumenta sua energia cinética e faz com que eles oscilem em torno de urna posição de equilíbrio média (círculos cheios), que é diferente para cada temperatura. A distância de ligação pode variar sobre toda a extensão das linhas horizontais, identificadas com o valor da temperatura, de T1 a T4 (temperaturas crescentes).
Na mitologia grega, Nióbia era a filha de Tãntalo, dois - Enem 2018
QuímicaNa mitologia grega, Nióbia era a filha de Tântalo, dois personagens conhecidos pelo sofrimento. O elemento químico de número atômico (Z) igual a 41 tem propriedades químicas e físicas tão parecidas com as do elemento de número atômico 73 que chegaram a ser confundidos.
Por isso, em homenagem a esses dois personagens da mitologia grega, foi conferido a esses elementos os nomes de nióbio (Z = 41) e tântalo (Z = 73). Esses dois elementos químicos adquiriram grande importância econômica na metalurgia, na produção de supercondutores e em outras aplicações na indústria de ponta, exatamente pelas propriedades químicas e físicas comuns aos dois.
Apoie nosso trabalho!
Assine Agora