Química
Exibindo questões de 1 a 100.
O uso de inibidores de proteínas permite estudar as funções dessas pro
QuímicaO uso de inibidores de proteínas permite estudar as funções dessas proteínas, como por exemplo, na cadeia respiratória mitocondrial. Nesse caso, o uso de inibidores específicos dos complexos proteicos da cadeia respiratória permite determinar o papel deles na fosforilação oxidativa. Para um ensaio experimental, os inibidores utilizados foram a rotenona, um inibidor do Complexo I, e o cianeto, um inibidor do Complexo IV.
Considerando o contexto apresentado pelo texto e seus conhecimentos sobre o assunto, analise as seguintes afirmativas:
I. O uso da rotenona ou do cianeto não interfere na fosforilação oxidativa, pois mesmo que os Complexos I e IV estejam inibidos, há ainda os Complexos II e III livres.
II. Com o uso do cianeto, o Complexo IV não consegue transferir seus elétrons para o oxigênio, por isso a fosforilação oxidativa é inibida.
III. No ensaio com a rotenona, a inibição do Complexo I da cadeia respiratória provocou reduções do consumo de gás oxigênio e da síntese de ATP.
IV. No ensaio com o cianeto, a inibição do Complexo IV da cadeia respiratória resultou na interrupção do consumo de gás oxigênio e da síntese de ATP.
Na fosforilação oxidativa, as reações de oxirredução possibilitam o
QuímicaNa fosforilação oxidativa, as reações de oxirredução possibilitam o fluxo de elétrons de NADH e FADH2 para o oxigênio. O fluxo de elétrons ocorre em quatro grandes complexos proteicos que estão inseridos na membrana interna da mitocôndria e juntos são denominados cadeia respiratória ou cadeia de transporte de elétrons. Três desses complexos proteicos utilizam a energia liberada pelo fluxo de elétrons para gerar um gradiente de pH e um potencial elétrico transmembrana que, por sua vez, geram a força próton-motriz. Essa força gera um fluxo de prótons, cuja energia é utilizada para formação de ATP. Portanto, a oxidação das fontes energéticas e a fosforilação do ADP para formar ATP são acopladas por um gradiente de prótons através da membrana mitocondrial interna.
O notável avanço no conhecimento sobre etiologia e patogênese das
QuímicaO notável avanço no conhecimento sobre etiologia e patogênese das neoplasias trouxe a constatação de que fatores genéticos e componentes ambientais, notadamente alguns vírus, certos agentes físicos e substâncias químicas variadas, têm papel no aparecimento de vários tumores humanos e de animais. Em outras palavras: os tumores são entendidos como o resultado de agressões ambientais em um indivíduo geneticamente suscetível. "
Com relação aos agentes carcinogênicos, associe a primeira coluna com a segunda coluna.
Primeira coluna:
A- Agente químico.
B- Agente físico.
C- Agente biológico.
Segunda coluna:
( ) radiação solar.
( ) vírus HPV.
( ) nitrosaminas.
( ) cigarro.
Muitas moléculas são classificadas como eletrólitos, isto é, podem
QuímicaMuitas moléculas são classificadas como eletrólitos, isto é, podem formar íons. Esse processo de ionização depende da participação da água. De acordo com as definições de Arrhenius, ácidos sofrem o processo de ionização quando adicionados em água e libera íons H+. A seguir são apresentadas substâncias classificadas como eletrólitos. I- HCI II- NH4* III-H2SO4 IV- NaOH
Os corpos cetônicos, produzidos predominantemente pelo fígado, são
QuímicaOs corpos cetônicos, produzidos predominantemente pelo fígado, são reservas energéticas plasmáticas
que podem ser utilizadas pelas células, especialmente as fibras musculares esquelética e cardíaca. Os
corpos cetônicos também têm importância clínica, pois estão associados ao quadro grave de cetoacidose
diabética.
Considerando as informações apresentadas e seus conhecimentos, analise as afirmativas a seguir.
1. Nas células, os corpos cetônicos sofrem cetólise para a liberação das moléculas de acetil-CoA para
posterior oxidação no ciclo do ácido cítrico.
II. Os hepatocitos e os eritrocitos são células que utilizam grandes quantidades de corpos cetônicos como
substratos energéticos.
III. No diabetes mellitus, devido à grande produção de corpos cetônicos pelas células, ocorre
cetonemia, ou seja, aumento dos níveis plasmáticos de corpos cetônicos.
IV. No jejum, mais ácidos graxos do tecido adiposo são mobilizados para compensar a hipoglicemia, com
consequente redução da cetogênese que depende da glicose.
A membrana plasmática, também conhecida como membrana celular, é uma e
QuímicaA membrana plasmática, também conhecida como membrana celular, é uma estrutura fina, com 7,5 a 10 nm de espessura, sendo uma barreira flexível e resistente que envolve o citoplasma celular. A descrição mais adequada é por meio de um modelo da estrutura da membrana denominada de mosaico fluido. A membrana plasmática é composta basicamente por proteínas, fosfolipídios, colesterol, lipídios e carboidratos. A estrutura da membrana plasmática é a bicamada lipídica, constituída basicamente três lipídios como, fosfolopídios, colesterol e glicolipídios.
Os átomos da molécula de CO2 estão unidos por
QuímicaAssinale a alternativa que corresponde a essa ligação.
Para o preparo de 1L (litro) de solução de Hidróxido de Sódio (NaOH) 1
QuímicaPara o preparo de 1L (litro) de solução de Hidróxido de Sódio (NaOH) 10mol/L [10M(molar)], é necessário
adicionar __________ de hidróxido de sódio (NaOH) em 500mL (mililitros) de água destilada e após,
Os átomos da molécula de CO2 estão unidos por um tipo de ligação
QuímicaOs átomos da molécula de CO2 estão unidos por um tipo de ligação química. Assinale a alternativa que corresponde a essa ligação.
Assinale o item que contém apenas ácido: a)H2S, NaC1, KOH b)HBr, HC1,
QuímicaAssinale o item que contém apenas ácido:
O forno de um cromatógrafo gasoso é um componente fundamental. Um
QuímicaO forno de um cromatógrafo gasoso é um componente fundamental. Um forno, quando bem regulado, reproduz a temperatura programada com precisão e rapidez. Outra função importante do forno na cromatografia gasosa é
O esquema a seguir representa o processo de extração do óleo essencial
QuímicaO esquema a seguir representa o processo de extração do óleo essencial de cascas de laranja
(Mack-SP) Considerando a pilha Znº/Zn2+ //Cu2+/Cu° e saben- do que o z
Química(Mack-SP) Considerando a pilha Znº/Zn2+ //Cu2+/Cu° e saben-
do que o zinco cede elétrons espontaneamente para íons
Cu2+,
Os lipídios abrangem uma classe de compostos orgânicos caracterizados
QuímicaOs lipídios abrangem uma classe de compostos orgânicos caracterizados pela alta solubilidade em solventes orgânicos não polares. Essa propriedade ocorre devido ao componente hidrocarboneto expressivo que também é responsável pela propriedade oleosa da molécula.
( ) Cadeia carbônica curta com número de carbonos entre 4-10.
( ) Cadeia carbônica média com número de carbonos entre 12-14.
( ) Cadeia carbônica longa com mais de 16 átomos de carbono.
Os monossacarídeos apresentam muitos carbonos assimétricos, o que
BASOs monossacarídeos ou açúcares simples são as menores unidades de açúcar que não podem ser hidrolisadas em carboidratos mais simples. Os monossacarídeos, compostos de função orgânica mista, são constituídos por um esqueleto carbônico de 3 a 7 carbonos. Os monossacarídeos apresentam muitos carbonos assimétricos, o que permite a formação de vários isômeros. Os isômeros são moléculas de mesma fórmula molecular, porém apresentam fórmulas estruturais diferentes e, por isso, propriedades diferentes.
A seguir, uma ilustração da estrutura de quatro monossacarídeos.
Fonte: elaborado pelo autor.
Considerando as informações apresentadas no texto e na figura, analise as afirmativas a seguir:
I. O monossacarídeo C corresponde ao isômero D, pois o grupo hidroxila do carbono assimétrico mais distante do grupo aldoxila está à direita. II. O monossacarídeo B corresponde a uma cetose, pois o grupo químico presente na estrutura é uma carbonila, que caracteriza a função orgânica cetona.
III. O monossacarídeo A corresponde a uma aldoxila, pois o grupo químico presente na estrutura é uma aldoxila, que caracteriza a função orgânica aldeído.
IV. O monossacarídeo D corresponde ao isômero L, pois o grupo hidroxila do carbono assimétrico mais distante do grupo aldoxila está à esquerda.
Os frascos para armazenamento de reagente e soluções geralmente são os
QuímicaOs frascos para armazenamento de reagente e soluções geralmente são os construídos em vidro, à base de borossilicatos ou com elevado teor de sílica, que apresentam boa resistência química e ao choque térmico. Considerando o texto anterior, analise as afirmações a seguir:
I. Frascos âmbar são geralmente utilizados para armazenar materiais que são sensíveis à luz.
II. Qualquer solução preparado em laboratório deve ser rotuladas com as seguintes informações: reagente químico, concentração, data de preparo e nome do analista que a preparou.
III. Soluções padrões devem ser mantidas sob refrigeração.
Ao realizarmos uma medida de massa, volume, dimensão, etc., sempre
QuímicaAo realizarmos uma medida de massa, volume, dimensão, etc., sempre haverá uma porcentagem de erro, ou melhor, sempre existirá uma determinada incerteza. Dependendo do instrumento utilizado para a medida, ela poderá ser mais precisa. Isso dependerá de sua incerteza. Por isso, é importante conhecermos quais algarismos são significados quando representamos um resultado de uma medição.
( ) A medida 0,023 g apresenta 4 algarismos significativos.
( ) A medida 2,300 g apresenta 4 algarismos significativos.
( ) A medida 0,5 mL apresenta 1 algarismo significativo.
A hipercalemia é resultado do aumento da concentração plasmática de
QuímicaA hipercalemia é resultado do aumento da concentração plasmática de ions potássio, quando a sua concentração
supera 5 mEq/L. A hipercalemia pode ser resultado de várias causas, como acidose metabólica ou respiratória, uso
de beta-bloqueadores (como o propranolol), intoxicação digitálica (toxicidade provocada pela digoxina),
insuficiência renal, administração excessiva de solução aquosa de KCl e o uso de diuréticos poupadores de potássio
(como a espironolactona). Entre as manifestações clínicas da hipercalemia, podemos destacar arritmias cardíacas,
risco alto de parada cardíaca, fraqueza, paralisia muscular, aumento da secreção de insulina pelas células beta-
pancreática com risco de hipoglicemia, confusão mental. O tratamento da hipercalemia depende da identificação e
resolução da causa. Porém, existem tratamentos para reverter a hipercalemia em casos de necessidade.
I. A solução polarizante é um dos tratamentos utilizados para a hipercalemia.
II. Diuréticos depletores de potássio auxiliam na redução dos níveis plasmáticos de potassio
III. A insulina estimula a captação de ions potássio pelas fibras musculares esqueléticas
IV. Uso de bicarbonato de sódio, ao elevar o pH sanguíneo, aumenta ainda mais a hipercalemia.
Considerando o contexto apresentado, é correto o que se afirma em
Escolha uma:
Entre os cátions, podemos destacar o sódio, o potássio, o cálcio, o
QuímicaEntre os cátions, podemos destacar o sódio, o potássio, o cálcio, o magnésio e o ferro. Entre os ânions, podemos destacar o cloreto, o iodeto e o fosfato. Esses minerais exercem funções importantes no organismo, como cofatores em várias reações químicas do metabolismo, transporte de gás oxigênio no sangue, armazenamento de energia nas células, contração muscular, geração e transmissão de impulsos nervosos e cardíacos, e tantas outras funções. De acordo com as informações apresentadas na tabela a seguir, faça a associação das funções na Coluna A com seus respectivos tipos de minerais, apresentados na Coluna B. COLUNA A COLUNA B I. Repolarização de neurônios e fibras musculares.
1. Sódio
II. Componente de hormônios tireoidianos. 2. Potássio
III. Manutenção do volume plasmático. 3. Iodo
IV. Antagonista do cálcio
O catabolismo de ácido graxo é chamado de beta-oxidação. É um processo
QuímicaO catabolismo de ácido graxo é chamado de beta-oxidação. É um processo repetitivo em 4 etapas que ocorre nas mitocôndrias, no qual os ácidos graxos são convertidos em moléculas de acetil-CoA. Os ácidos graxos ficam armazenados nos adipócitos na forma de triacilgliceróis e, quando mobilizados, são oxidados, principalmente pelas fibras musculares, para a produção de energia. A oxidação completa de um grama de ácidos graxos gera mais do que o dobro de energia do que a oxidação completa de um grama de glicose.
O estágio 1 consiste na geração de uma molécula central composta por
QuímicaO estágio 1 consiste na geração de uma molécula central composta por dois carbonos, acetil-CoA. O estágio 2 é a oxidação da acetil-CoA no ciclo de Krebs. O estágio 3 é o processo de fosforilação oxidativa (i. E. , formação de ATP) na cadeia de transporte de elétrons (i. E. , cadeia respiratória)". Com base neste trecho, julgue as afirmativas a seguir em (V) Verdadeiras ou (F) Falsas.
( ) As etapas descritas referem-se a uma via anaeróbia.
( ) O mecanismo descrito resulta em 2 ATPs.
( ) A via energética descrita envolve a quebra de micronutrientes no estágio
Os elementos fundamentais no processo de obtenção de imagens
QuímicaOs elementos fundamentais no processo de obtenção de imagens radiológicas desempenham um papel crucial na garantia de diagnósticos médicos precisos e seguros. O tubo de raios-X, responsável por gerar feixes de radiação, e o colimador, que controla sua direção, desempenham um papel essencial na minimização da exposição desnecessária, destacando a importância da precisão na prática diagnóstica. Os detectores eletrônicos têm a função de converter os raios-X em sinais digitais, possibilitando a criação de imagens digitais avançadas, um avanço tecnológico significativo no campo da radiologia. A relevância destes componentes é evidenciada não apenas pela precisão diagnóstica, mas também pela priorização da segurança do paciente, reduzindo a exposição à radiação. O contínuo avanço tecnológico desses elementos tem um impacto positivo na melhoria constante da prática radiológica, resultando em uma assistência médica de maior qualidade.
O entendimento da estrutura da matéria não foi importante apenas para
QuímicaO entendimento da estrutura da matéria não foi importante apenas para satisfazer a curiosidade dos cientistas, ela é importante para a produção de novas tecnologias e materiais. Tal descoberta foi iniciada por Dalton (1766-1844) quando resgatou as ideias sobre o átomo, introduzidas por Demócrito e Leucipo, contemporâneos de Aristóteles.
Com relação a ligações químicas, eletronegatividade, repulsão de pares
QuímicaCom relação a ligações químicas, eletronegatividade, repulsão de pares eletrônicos e geometria molecular, marque a alternativa correta.
A radiação ionizante é um tipo de energia que, ao interagir com
QuímicaA radiação ionizante é um tipo de energia que, ao interagir com a matéria, tem a capacidade de remover elétrons dos átomos, criando íons carregados. Ela pode ser corpuscular ou eletromagnética. A radiação corpuscular é constituída por partículas eletricamente carregadas. Esse tipo de radiação, ao interagir com a matéria transfere energia suficiente para remover um elétron do átomo de forma direta. Dentro dessa classificação é possível dividir em partículas carregadas pesadas (exemplo: radiação alfa - a) ou em partículas leves (exemplo: radiação beta - ß). A radiação eletromagnética pertence a classe da radiação indiretamente ionizante e é representada por fótons de raios X oriundos de excitações atômicas e da desaceleração de partículas carregadas e raios gama (¿) originados de desexcitações nucleares por exemplo. Esse tipo de radiação ao interagir com moléculas da matéria, por meio da ação de campos eletromagnéticos, forma espécies reativas que, por sua vez, ionizam átomos adjacentes. Compreender as propriedades dos tipos de interação da radiação com a matéria é importante para aplicação na prática radiológica.
As ciclodextrinas são oligossacarídeos cíclicos também chamados de
QuímicaAs ciclodextrinas são oligossacarídeos cíclicos também chamados de dextrinas e cicloamiloses, compostas por unidades de α-D-glicopiranosil unidas por ligações 1 → 4. Elas podem ser formadas a partir de polímeros de amido solúvel. Sua aplicação em alimentos se deve a sua habilidade de formar complexos.
O valor do pH de uma amostra indica o estado de equilíbrio ácidobase.
QuímicaO valor do pH de uma amostra indica o estado de equilíbrio ácidobase. Um pH normal demonstra a ausência de desvios ou sua completa compensação. Se o pH está abaixo de 7,35, dizemos que existe acidose, quando o pH está acima de 7,45, dizemos que existe alcalose. Agora calcule o pH de uma solução-tampão formada pela mistura de solução com 0,1 M de ácido acético e solução com 0,5 M de acetato de sódio.
Dados: Ka do ácido acético = 1,8. 10-5; log 1,8 = 0,25 e log 5 = 0,7.
Ao desenharmos um orbital atômico, damos a ideia que sua fronteira
QuímicaAo desenharmos um orbital atômico, damos a ideia que sua fronteira é bem definida, entretanto isso não ocorre, não podemos dizer exatamente que o elétrons de um átomo chegam somente até aquele ponto, nem matematicamente e nem com observações diretas. Porém podemos utilizar de medidas indiretas para conseguirmos estas informações.
Como por exemplo, analisar moléculas compostas pelos mesmos átomos. Neste caso, a definição de raio atômico é dada como metade da distância entre os centros de dois átomos.
Exemplos de raio atômico Quando um átomo perde elétrons, ele passa a ter uma carga positiva (__________) e é sempre ________ que o átomo neutro do elemento que o originou. Quando um átomo ganha um elétron, ele passa a ter uma carga negativa e é chamado de ________. Sendo sempre ___________ que o átomo que o originou.
"A via catabólica da(o) corresponde a uma sequência repetida de
Química"A via catabólica da(o) corresponde a uma sequência repetida de 4 reações ou etapas que envolvem o carbono beta (carbono 3) da cadeia de ácido graxo, resultando na redução da cadeia de ácido graxo em carbonos: o acetil-CoA".
A tabela periódica é dividida em grupos de elementos que apresentam
QuímicaA tabela periódica é dividida em grupos de elementos que apresentam características em comum, sendo comumente separados em metais, metaloides e não metais. Sobre a tabela periódica, analise as afirmativas a seguir:
I- Os elementos de transição utilizam uma subcamada d para acomodar os elétrons mais energéticos, enquanto os elementos de transição interna (lantanídeos e actinídeos) utilizam a camada p.
II- A tabela periódica possui duas linhas fora da tabela. As características desses elementos são muito comuns entre cada linha, sendo cada linha chamada de série. A primeira linha corresponde aos elementos da série lantanídeos e a segunda série dos actinídeos.
III- Os elementos da última coluna da tabela periódica correspondem aos gases nobres, que possuem sua camada de valência preenchida por oito elétrons, dois no caso do elemento hélio.
A solubilidade de uma solução é a propriedade que relaciona
QuímicaA solubilidade de uma solução é a propriedade que relaciona a capacidade que uma substância tem de se dissolver em outra. Essa grandeza é medida de acordo com a concentração de saturação da solução.
A síntese de amônia é o processo industrial mais importante para
QuímicaA síntese de amônia é o processo industrial mais importante para o isolamento do nitrogênio, assim como para produção adicional de compostos nitrogenados de importância vital (ureia, ácido nítrico e fertilizantes). Este processo é quase centenário, tendo sido descoberto no início do século 20 por Fritz Haber e desenvolvido para a produção industrial por Carl Bosch.”
OLIVEIRA, L. C. A.; FABRIS, J. D.; PEREIRA, M. C. Óxidos de ferro e suas aplicações em processos catalíticos: uma revisão. Química Nova, São Paulo, v. 36, n. 1, p. 123-130, 2013.
A síntese da amônia pode ser expressa pela seguinte reação:
N subscript 2 space subscript left parenthesis g right parenthesis end subscript space plus space 3 space H subscript 2 space left parenthesis g right parenthesis end subscript space rightwards harpoon over leftwards harpoon space 2 space N H subscript 3 space left parenthesis g right parenthesis end subscript
Considerando essa síntese, complete as lacunas da sentença a seguir com os termos corretos:
Caso sejam adicionados 28 gramas de N2 e 10 gramas de H2, pode-se afirmar que o gás nitrogênio é o reagente ____________ e o hidrogênio é o reagente ____________.
Dados: MMNitrogênio: 14 g/mol e MMHidrogênio: 1 g/mol.
Uma mistura de 0,1 mol L-1 de um ácido X e 0,5 mol L-1 de substância Y
QuímicaUma mistura de 0,1 mol L-1 de um ácido X e 0,5 mol L-1 de substância Y, constitui uma solução-tampão. Sabendo que a Ka do ácido X é de 1,8 x 10-5; e considerando o log de 1,8 igual a 0,25 e o log de 5 igual a 0,7, o pH da solução em questão é de?
O projeto molecular de novos medicamentos pode adotar uma abordagem
QuímicaO projeto molecular de novos medicamentos pode adotar uma abordagem fisiológica. A concepção estrutural da molécula baseia-se na compreensão do mecanismo de intervenção terapêutica, o qual está ligado à escolha do alvo terapêutico. Para selecionar o alvo ideal, é essencial compreender o processo fisiopatológico da doença.
Sobre o exposto, avalie as afirmativas a seguir e marque V para as verdadeiras e F para as falsas.
( ) Bioisosterismo é a modificação racional de um composto protótipo, através da troca de determinado fragmento molecular por outro, que apresente propriedades físico-químicas semelhantes.
( ) Os anéis aromáticos não estão presentes na maioria das estruturas de interesse terapêutico. São raros os fármacos que apresentam unidades aromáticas em sua estrutura.
( ) Substâncias químicas bioativas possuem várias regiões de interação intermolecular, que são importantes para definir a sua atividade farmacológica.
Compostos iônicos não são moléculas, ou seja, não são pares ânions
QuímicaCompostos iônicos não são moléculas, ou seja, não são pares ânions-cátions isolados, e sim íons arranjados em um retículo tridimensional, sendo que cada íon está em contato com mais de um vizinho. A estrutura de cada retículo depende da carga dos íons e de seus tamanhos. Embora NaCl seja representado como molécula, precisamos saber que esta é na verdade a proporção entre e no retículo. Sobre compostos iônicos, a alternativa que contém uma afirmação correta é:
Os ácidos graxos são moléculas formadas por um esqueleto
QuímicaOs ácidos graxos são moléculas formadas por um esqueleto hidrocarbônico, com 4 a 36 átomos de carbono de comprimento, e um grupo carboxila na extremidade da cadeia. As ligações entre os carbonos podem ser simples, no caso dos ácidos graxos saturados, ou duplas, no caso dos ácidos graxos insaturados. Quando houver apenas uma única ligação dupla entre os carbonos, o ácido graxo é chamado de monoinsaturado. No caso de haver duas ou mais ligações duplas entre os carbonos, o ácido graxo é chamado de poli-insaturado. Os ácidos graxos, como são apolares, interagem entre si por meio das ligações de van der Waals entre as cadeias hidrocarbônicas.
Com base na estrutura química dos ácidos graxos, avalie as seguintes asserções e a relação proposta entre elas.
I. Em temperatura ambiente, os compostos com predomínio de ácidos graxos saturados, especialmente os com cadeia hidrocarbônica de maior comprimento, são líquidos. Isso ocorre devido ao menor número de ligações de van der Waals entre as cadeias hidrocarbônicas de ácidos graxos adjacentes.
PORQUE
II. O ponto de fusão dos ácidos graxos aumenta com o comprimento da cadeia hidrocarbônica e diminui na presença de ligações duplas entre os carbonos da cadeia hidrocarbônica. O ponto de fusão do composto formado por ácidos graxos depende da quantidade de ligações de van der Waals entre as cadeias hidrocarbônicas de ácidos graxos adjacentes, bem como da temperatura do ambiente.
Uma salina é uma área que produz sal a partir de sua extração da água
QuímicaUma salina é uma área que produz sal a partir de sua extração da água do mar, e o processo de precipitação destes sais se dá, a grosso modo, a partir da evaporação e purificação de sua água. Como as águas das salinas são soluções aquosas, os conceitos de solubilidade e soluções são aplicáveis.
Uma solução analítica foi preparada pela dissolução de 1,23 x 1024
QuímicaUma solução analítica foi preparada pela dissolução de 1,23 x 1024 átomos de hidróxido de sódio em um litro de água. Para o preparo dessa solução, assinale a alternativa que apresenta o número de mols de NaOH utilizado. Dados: 1 mol = 6,022 x 1023 átomos.
Em um frasco “A” estão apenas moléculas de metano (CH4), de geometria
QuímicaEm um frasco “A” estão apenas moléculas de metano (CH4), de geometria tetraédrica. Em outro frasco, B, estão apenas moléculas de clorofórmio (CHCl3), também de geometria tetraédrica. Quando estas substâncias estiverem no estado líquido, serão unidas, respectivamente, por:
Reações de substituição nucleofílica ocorrem por meio de um mecanismo
QuímicaReações de substituição nucleofílica ocorrem por meio de um mecanismo iônico. Nestas reações, uma molécula rica em elétrons, denominada nucleófilo substitui um dos ligantes em uma molécula orgânica em uma posição eletrófila, que é uma região pobre em elétrons, originando uma nova molécula orgânica. Sobre as reações de substituição nucleofilica, avalie as afirmativas a seguir:
I- As reações de substituição nucleofilica podem ocorrer por meio de um mecanismo unimolecular e por melo de um mecanismo bimolecular.
II- Na reação de substituição nucleofilica unimolecular, o grupo de saída presente na molécula é substituido por um nucleófilo em duas ou mais etapas de reação que envolvem, geralmente, a perda da memória estérica, caso a molécula apresente estereoisomeria.
III- A reação de substituição nucleofilica unimolecular ocorre em uma única etapa, em que a entrada do nucleófilo e a perda do grupo de saida ocorrem em apenas uma etapa.
Na reação de Friedel-Crafts, ocorre a alquilação do benzeno, em que
QuímicaNa reação de Friedel-Crafts, ocorre a alquilação do benzeno, em que um grupo alquila R é introduzido pela reação com R – Cl, na presença de AlCl₃. Quando já há a presença de um grupo ligado ao benzeno, a reatividade pode variar, dependendo do grupo ligado. Qual substituinte ligado ao benzeno poderá provocar um aumento da reatividade em uma reação de Friedel-Crafts?
Assinale a opção que apresenta somente membros do grupo 1 da tabela
QuímicaAssinale a opção que apresenta somente membros do grupo 1 da tabela periódica.
No estudo de um novo medicamento, uma molécula foi isolada e a sua
QuímicaNo estudo de um novo medicamento, uma molécula foi isolada e a sua composição passou por uma análise centesimal. Através da análise foram obtidos os seguintes resultados: - 64,3% de Carbono - 7,1% de Hidrogênio - 17,1% de Oxigênio - 11,4% de Enxofre Sabendo que 500g do composto foram analisados e sua massa molecular é igual a 280 g/mol, assinale a alternativa que apresenta a sua fórmula molecular.
Um analista de laboratório precisa determinar a determinação de um
QuímicaUm analista de laboratório precisa determinar a determinação de um parâmetro biológico na urina de um paciente. A coleta da urina seguiu os protocolos estabelecidos pelo hospital e a amostra foi encaminha para realização de exames bioquímicos. Para determinação de uma proteína presente na urina, o analista precisa selecionar um volume de 10 mL, com a máxima precisão possível, e transferir para um tubo de análise. A análise em questão é extremamente rara de ser realizada e o laboratório não possui um protocolo definido, dessa forma, o analista resolveu realizar uma análise exploratório, e a partir do resultado encontrado, coletar novas amostras para encaminhar para um laboratório que possui a análise credenciada. Para seleção do volume, o analista possui os seguintes materiais:
1-Pipeta graduada de 5 mL
2-Pipeta graduada de 10 mL
3-Pipeta volumétrica de 10 mL
4-Proveta de 50 mL
5-Proveta de 10 mL
Ligação química corresponde a união entre átomos para formar novas
QuímicaLigação química corresponde a união entre átomos para formar novas substâncias químicas. Um analista precisa selecionar um composto, entre uma série de substâncias presentes em seu almoxarifado para formar uma solução iônica que será empregado para fornecer força iônica a um determinado processo laboratorial, para isso, um sal deverá ser dissolvido em água e originar uma solução saturada. Sobre o exposto, assinale a alternativa que apresenta uma substância química que ao ser adicionada em água, irá originar uma solução iônica.
A matéria, segundo a química, é definida como tudo que possui massa
QuímicaA matéria, segundo a química, é definida como tudo que possui massa e ocupa lugar no espaço, além disso, ela pode se apresentar em diferentes estados físicos. Estes estados estão relacionados com a configuração macroscópica que os átomos podem apresentar. Sobre os estados físicos da matéria, assinale a alternativa que denomina corretamente o estado que é caracterizado por possui volume definido e forma indefinida.
A meia-vida é uma propriedade relacionada a substâncias químicas
QuímicaA meia-vida é uma propriedade relacionada a substâncias químicas e que descreve o tempo necessário para que metade dos átomos (ou metade da massa) presentes em uma amostra seja desintegrada.
Considere que uma substância possua uma meia-vida de 8 horas. Se a amostra inicial apresenta massa de 500 mg, após quanto tempo a quantidade de substância será reduzida para apenas 62,5 mg?
O modelo atômico de Bohr permitiu a Mendeleev estabelecer a tabela
QuímicaO modelo atômico de Bohr permitiu a Mendeleev estabelecer a tabela periódica.
O hélio é o único gás nobre que não tem 8 elétrons em sua camada de
QuímicaO hélio é o único gás nobre que não tem 8 elétrons em sua camada de valência.
No processo de oxidação, ocorre a adição de elétrons em um átomo.
QuímicaNo processo de oxidação, ocorre a adição de elétrons em um átomo.
A energia de ionização é aquela liberada quando um átomo isolado
QuímicaA energia de ionização é aquela liberada quando um átomo isolado no estado fundamental, em fase gasosa, recebe um elétron.
A configuração eletrônica do íon metálico do complexo em apreço
QuímicaA configuração eletrônica do íon metálico do complexo em apreço termina em um orbital d8.
Considere um elemento químico, genericamente nomeado X. Sua massa
QuímicaConsidere um elemento químico, genericamente nomeado X. Sua massa é igual a 56 e o número de nêutrons igual a 30. O número de elétrons desse elemento químico em estado X2+ será:
O modelo atômico de Rutherford-Bohr considera a existência de
QuímicaO modelo atômico de Rutherford-Bohr considera a existência de orbitais circulares e elípticos, e o núcleo do átomo é composto por prótons e nêutrons.
Conforme o modelo atômico de Dalton, também conhecido como modelo
QuímicaConforme o modelo atômico de Dalton, também conhecido como modelo pudim de passas, o átomo é tal qual uma esfera de material gelatinoso com carga positiva sobre a qual os elétrons ficam suspensos.
Considerando-se a estrutura atômica, marcar C para as afirmativas
QuímicaConsiderando-se a estrutura atômica, marcar C para as afirmativas Certas, E para as Erradas e, após, assinalar a alternativa que apresenta a sequência CORRETA:
( ) Ao atritarmos uma bexiga de balão cheia ao cabelo, a bexiga fica eletrizada negativamente, passando a exercer uma força atrativa entre os dois objetos.
( ) Um bastão de vidro atritado a um pedaço de lã e, em seguida, aproximado a pedacinhos de papel, passa a exercer uma força de repulsão.
( ) Elementos como o enxofre (S) e cobre (Cu) são bons condutores de corrente elétrica; ambos são metais.
( ) Elementos como Mg e Ca têm tendência a perder elétrons, enquanto elementos como Br e Cl têm tendência a ganhar elétrons.
O CO2 e o NO2 possuem estruturas moleculares diferentes entre si.
QuímicaO CO2 e o NO2 possuem estruturas moleculares diferentes entre si. Assinale a alternativa correta sobre as estruturas das moléculas descritas acima.
No cultivo por hidroponia, são utilizados soluções nutritivas contendo
QuímicaNo cultivo por hidroponia, são utilizados soluções nutritivas contendo macronutrientes e micronutrientes essenciais. Além dos nutrientes, o pH é um parâmetro de extrema importância, uma vez que ele afeta a preparação da solução nutritiva e a absorção dos nutrientes pelas plantas. Para o cultivo de alface, valores de pH entre 5,5 e 6,5 são ideais para o seu desenvolvimento. As correções de pH são feitas pela adição de compostos ácidos ou básicos, mas não devem introduzir elementos nocivos às plantas. Na tabela, são apresentados alguns dados da composição da solução nutritiva de referência para esse cultivo. Também é apresentada a composição de uma solução preparada por um produtor de cultivo hidropônico.
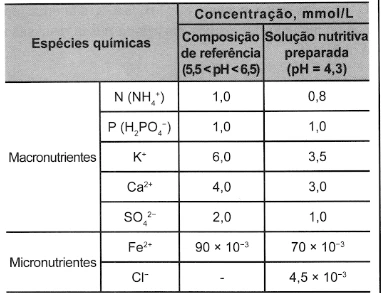
LENZI, E; FAVERO, L. O. B; LUCHESE, E. B. Introdução à química da água: ciência, vida e sobrevivência. Rio de Janeiro: LTC, 2012 (adaptado).
Em uma situação em que a ingestão de carboidrato supera a necessidade
QuímicaEm uma situação em que a ingestão de carboidrato supera a necessidade orgânica, as células desviam parte da glicose absorvida para uma via alternativa. Nessa via ocorre a participação de NADPH que possui função oposta ao NAD+. Qual o nome dessa via?
O piruvato formado no final da glicólise é uma molécula de 3 carbonos
QuímicaO piruvato formado no final da glicólise é uma molécula de 3 carbonos que participa de diversos destinos. Qual alternativa não apresenta um dos destinos do piruvato?
A ligação química é a força atrativa entre dois átomos, resultante
QuímicaA ligação química é a força atrativa entre dois átomos, resultante da reorganização dos elétrons de suas camadas de valência. Sobre as ligações químicas, avalie os compostos apresentados a seguir.
I- Cloreto de sódio, NaCl.
II- Água, H2O.
III- Etanol, C2H6O.
IV- Hidróxido de sódio, NaOH.
Gilbert Newton Lewis (1875-1946) foi um importante químico que estudou
QuímicaGilbert Newton Lewis (1875-1946) foi um importante químico que estudou as ligações químicas. Através de seus estudos desenvolveu uma teoria de ligação com base no número de elétrons na camada de valência do átomo. Tomando como referência os conceitos de ligação química, julgue as afirmativas a seguir em (V) Verdadeiras ou (F) Falsas.
( ) Uma ligação química corresponde a atração química entre átomos iguais ou diferentes, que pode ser devido ao compartilhamento de elétrons, transferência de elétrons ou apenas por força atrativa mantendo átomos unidos.
( ) A ligação covalente é resultado da transferência de elétrons de um átomo metálico para um não-metálico.
( ) Quando dois átomos similares se unem por uma ligação covalente, nenhum deles quer ganhar ou perder elétron para atingir a regra do octeto.
( ) A ligação iônica (primária) ocorre pela associação das eletrosferas de átomos de cargas semelhantes ou iguais.
A degradação dos lipídeos envolve uma série de reações enzimáticas
QuímicaA degradação dos lipídeos envolve uma série de reações enzimáticas capazes de garantir uma grande quantidade de energia por ácido graxo, isso porque:
I- A degradação dos lipídeos envolve três fases, entre elas a β-oxidação.
II- A β-oxidação é medida por ação de enzimas denominadas Acil-CoA sintetases.
III- As enzimas Acil-CoA têm por finalidade elongar a cadeia do ácido graxo, garantindo maior quantidade de energia por molécula de gordura.
IV- A degradação dos ácidos graxos converge com a degradação dos carboidratos.
A respiração é fundamental para a sobrevivência do ser humano, pois
QuímicaA respiração é fundamental para a sobrevivência do ser humano, pois este sistema é responsável por trocar os gases: oxigênio (O2) e dióxido de carbono (CO2). Para que os gases respiratórios possam alcançar os tecidos do nosso corpo e ocorrer as trocas gasosas é necessário que estes sejam transportados ao longo dos vasos sanguíneos. De acordo com o transporte dos gases, julgue as afirmativas a seguir em (V) Verdadeiras ou (F) Falsas.
( ) O dióxido de carbono se transforma em bicarbonato para ser transportado pelo sangue.
( ) O oxigênio utiliza uma proteína para ser transportado no sangue.
( ) O dióxido de carbono é transportado em sua maior parte dissolvido no sangue.
( ) A hemoglobina é uma proteína presente no sangue responsável por transportar os gases.
Muitas substâncias consideradas tóxicas têm aplicações terapêuticas
QuímicaMuitas substâncias consideradas tóxicas têm aplicações terapêuticas quando utilizadas em mínimas doses. Exemplo dessa propriedade é o flúor. Embora considerado muito venenoso, é um bom fármaco contra as cáries. Para Paracelsus (1493-1541) "a dose certa diferencia o veneno do remédio". De acordo com o Ministério da Saúde, o limite máximo de flúor na água para consumo humano é de 1,5 mg/L. Quantos mililitros de água seriam necessários para preparar uma solução, de acordo com o limite máximo permitido, contendo 400 μg de flúor?
O ciclo do ácido cítrico é um conjunto de reações químicas que ocorre
QuímicaO ciclo do ácido cítrico é um conjunto de reações químicas que ocorre na matriz mitocondrial e corresponde à última etapa oxidativa de diferentes vias produtoras de energia do organismo. As reações desse ciclo fornecem uma grande quantidade de elétrons e energia para o organismo. Sobre o ciclo do ácido cítrico, assinale a alternativa que apresenta os produtos obtidos após uma volta completa nesse ciclo.
Minerais são amplamente distribuídos nos alimentos, sendo uma
QuímicaMinerais são amplamente distribuídos nos alimentos, sendo uma alimentação bem equilibrada suficiente para fornecer todos os minerais nas suas quantidades adequadas para o metabolismo do organismo. Sobre o exposto, assinale a alternativa que denomina o mineral que é componente da hemoglobina, presente nos eritrócitos, que é responsável pela interação com o oxigênio.
Lipoproteínas plasmáticas são formadas por lipídeos complexos e por
QuímicaLipoproteínas plasmáticas são formadas por lipídeos complexos e por proteínas específicas. Sobre a lipoproteína LDL (lipoproteína de baixa densidade), assinale a alternativa correta.
Carboidratos correspondem as biomoléculas mais abundantes na Terra
QuímicaCarboidratos correspondem as biomoléculas mais abundantes na Terra, além disso, possuem grande diversidade estrutural, podendo apresentar diferentes funções no organismo, como fonte e reserva de energia. Sobre os carboidratos, avalie as assertivas a seguir e as relações entre elas.
I- O glicogênio é um polissacarídeo que atua como armazenamento de glicose nas células animais.
PORQUE,
II- O glicogênio é um polissacarídeo de glicose formado por ligações glicosídicas do tipo (beta 1 – 4).
No ciclo da conscientização sobre a importância da - MACKENZIE
QuímicaNo ciclo da conscientização sobre a importância da preservação dos mananciais e do uso e trato adequado da água, o Brasil deve se destacar, visto ser depositário da maior reserva de água doce, líquida, do mundo. A presença de determinadas espécies químicas na água, em concentrações elevadas, interfere muito na sua qualidade.
A água é uma molécula que apresenta fórmula molecular H2O. Ela se
QuímicaA água é uma molécula que apresenta fórmula molecular H2O. Ela se encontra distribuída por todo o planeta e está presente no solo, na crosta terrestre em rios, lagos, mares e geleiras e na atmosfera. A água é fundamental para a vida como nos a conhecemos. Sobre a molécula de água, avalie as afirmativas a seguir:
I- A molécula de água é apolar, desse modo, ele sofre diferentes tipos de interações intermoleculares, como as ligações de hidrogênio e as interações de London.
II- Algumas propriedades da água, como o estado físico e a tensão superficial estão diretamente relacionadas as ligações de hidrogênio que ocorre entre as moléculas de água.
III- Na superfície, as moléculas de água interagem mais fortemente com as moléculas de água vizinhas, formando um tipo de película que possui resistência a deformação.
As reações químicas do metabolismo estão organizadas em vias
QuímicaQuando moléculas, átomos ou íons aproximam-se uns dos outros, dois
QuímicaQuando moléculas, átomos ou íons aproximam-se uns dos outros, dois fenômenos podem ocorrer: (i) eles podem reagir ou (ii) eles podem interagir. Uma reação química por definição requer que ligações químicas sejam quebradas e/ ou formadas. Usualmente as energias envolvidas neste processo variam entre 50 e 100 kcal.mol-1. Uma interação química significa que as moléculas se atraem ou se repelem entre si, sem que ocorra a quebra ou formação de novas ligações químicas. Estas interações são frequentemente chamadas de interações não covalentes ou interações intermoleculares.
Fonte: ROCHA, W. R. Interações intermoleculares. Química Nova na Escola, n. 4, p. 31-36, 2001.
Considerando esse contexto, avalie as seguintes asserções e a relação proposta entre elas:
I - Quanto mais intensas as interações intermoleculares, maior deverá ser o ponto de fusão.
PORQUE
II- Quanto maior a interação entre as moléculas, mais energia deve ser fornecida ao sistema para romper as interações molécula-molécula e então passar à fase vapor.
O uso de inibidores de proteínas permite estudar as funções dessas
BASO uso de inibidores de proteínas permite estudar as funções dessas proteínas, como por exemplo, na cadeia respiratória mitocondrial. Nesse caso, o uso de inibidores específicos dos complexos proteicos da cadeia respiratória permite determinar o papel deles na fosforilação oxidativa. Para um ensaio experimental, os inibidores utilizados foram a rotenona, um inibidor do Complexo I, e o cianeto, um inibidor do Complexo IV.
Considerando o contexto apresentado pelo texto e seus conhecimentos sobre o assunto, analise as seguintes afirmativas:
I. O uso da rotenona ou do cianeto não interfere na fosforilação oxidativa, pois mesmo que os Complexos I e IV estejam inibidos, há ainda os Complexos II e III livres.
II. Com o uso do cianeto, o Complexo IV não consegue transferir seus elétrons para o oxigênio, por isso a fosforilação oxidativa é inibida.
III. No ensaio com a rotenona, a inibição do Complexo I da cadeia respiratória provocou reduções do consumo de gás oxigênio e da síntese de ATP.
IV. No ensaio com o cianeto, a inibição do Complexo IV da cadeia respiratória resultou na interrupção do consumo de gás oxigênio e da síntese de ATP.
O sistema tegumentar é formado pela pele e anexos cutâneos e apresenta
QuímicaO sistema tegumentar é formado pela pele e anexos cutâneos e apresenta funções complexas e muito importantes, como: a proteção contra impactos, microrganismos e radiação ultravioleta, impermeabilizar a superfície da pele, participar da regulação da temperatura corporal e da sensibilidade cutânea. Os anexos da pele são as unhas, os pelos e as glândulas sudoríparas, as glândulas sebáceas com seus respectivos ductos. Se encontram entre as diferentes camadas da pele sendo elas vascularizadas ou não. RIEGER. Érica. Princípios de Química e Cosmetologia. Maringá: Unicesumar, 2019. Sobre os anexos da pele, suas partes e características, assinale V para verdadeiro e F para falso:
( ) As lâminas ungueais ou também chamadas de apenas unhas, auxiliam no ato de pegar objetos e realizar movimentos finos. São formadas por queratina dura e semitransparente.
( ) Os pelos estão presentes em grande parte da extensão cutânea: são estruturas sensoriais, de proteção e estão associados à imagem pessoal, representando força e poder. É por meio dos pelos que se sente o leve toque, como de um inseto e que tem-se a proteção contra microrganismos e partículas estranhas.
( ) A anatomia da unha conta com raiz, corpo, leito ungueal, bordas ungueais, eponíqueo (cutícula) e lúnula.
( ) As glândulas sebáceas desemboca na superfície da pele e tem por objetivo resfriar e manter o controle da temperatura, interferindo na hidratação cutânea.
( ) A hipoderme se encontra abaixo da derme, também chamada de tela subcutânea. É formada por tecido conjuntivo frouxo, a hipoderme está presente em maior quantidade no sexo masculino e armazena a maioria dos triglicerídeos.
As células típicas dos tecidos ósseo, cartilaginoso e nervoso recebem
QuímicaAs células típicas dos tecidos ósseo, cartilaginoso e nervoso recebem, a denominação de:
A lipogênese ocorre no citosol das células adiposas. Quando há uma
QuímicaA lipogênese ocorre no citosol das células adiposas. Quando há uma grande formação de citrato na mitocôndria, ele é lançado para o citoplasma, onde ocorrerá uma reação de separação do citrato em oxaloacetato e Acetil-Coa. Em resumo, podemos falar que a relação ADP/ATP é responsável pelo direcionamento das reações de degradação ou síntese. Assim, é correto dizer que para a lipogênese é importante que a relação ADP/ATP seja:
Em uma atividade física intensa e prolongada, a pessoa começa
QuímicaEm uma atividade física intensa e prolongada, a pessoa começa a sentir dores musculares, cãibras e fadiga. Um dos responsáveis por esse quadro é o acúmulo de lactato ou ácido láctico, decorrente de um fluxo sanguíneo insuficiente para atender as demandas metabólicas dos músculos esqueléticos. Considerando as informações apresentadas e nos seus conhecimentos sobre o assunto, analise as afirmativas a seguir:
I. Em situação de anóxia ou hipóxia, ocorre acúmulo de NADH e consumo de NAD+. Esse desequilíbrio entre as quantidades de NADH e NAD+ inibe a glicólise, a única via produtora de energia que não precisa de oxigênio.
II. Durante o repouso, o lactato formado durante a fermentação não tem utilidade para o organismo, precisando ser eliminado para evitar o seu acúmulo no sangue. O risco é de acidemia, por isso, o lactato é totalmente eliminado pela urina.
III. Na fermentação, o piruvato é reduzido à lactato, em uma reação catalisada pela lactato desidrogenase, permitindo a oxidação de NADH à NAD+. Com NAD+ disponível, a glicólise continua funcionando nas células.
IV. O lactato formado durante a fermentação é removido da circulação sanguínea pelo fígado, onde é substrato para a gliconeogênese. Em seguida, a glicose formada no fígado é utilizada para repor o estoque de glicogênio nos músculos. Esse é o ciclo de Cori.
Os glicosaminoglicanos polissacarídeos formados por repetições de uma
Aap2Os glicosaminoglicanos polissacarídeos formados por repetições de uma unidade dissacarídica composta por um açúcar ácido e um açúcar aminado. O açúcar ácido pode ser o ácido D-glicurônico e o ácido aminado pode ser a D-glicosamina. Esses açúcares são produtos de modificações químicas na glicose, com a adição de grupo carboxila para formar açúcar ácido e de grupo amino para formar açúcar aminado.
Com base na estrutura química dos glicosaminoglicanos, avalie as seguintes asserções e a relação proposta entre elas.
Os glicosaminoglicanos são heteropolissacarídeos com grande quantidade de cargas negativas. Devido à essa natureza negativa, as cadeias de glicosaminoglicanos mantêm-se estendidas e envolvidas por moléculas de água. Isso garante a viscosidade, lubrificação, adesão e resistência à compressão das secreções da mucosa, do fluido sinovial e da matriz extracelular.
PORQUE
Os glicosaminoglicanos possuem na sua estrutura dois tipos de monossacarídeos modificados a partir da glicose, o ácido D-glicurônico e o a D-glicosamina. O ácido D-glucurônico possui grupo carboxila na sua estrutura que, em pH neutro, possui carga negativa. Dessa maneira, as moléculas de água são atraídas pelas cargas negativas das carboxilas, permitindo uma concentração de água no meio ao redor das moléculas de glicosaminoglicanos.
Na fosforilação oxidativa, as reações de oxirredução possibilitam
QuímicaNa fosforilação oxidativa, as reações de oxirredução possibilitam o fluxo de elétrons de NADH e FADH2 para o oxigênio. O fluxo de elétrons ocorre em quatro grandes complexos proteicos que estão inseridos na membrana interna da mitocôndria e juntos são denominados cadeia respiratória ou cadeia de transporte de elétrons. Três desses complexos proteicos utilizam a energia liberada pelo fluxo de elétrons para gerar um gradiente de pH e um potencial elétrico transmembrana que, por sua vez, geram a força próton-motriz. Essa força gera um fluxo de prótons, cuja energia é utilizada para formação de ATP. Portanto, a oxidação das fontes energéticas e a fosforilação do ADP para formar ATP são acopladas por um gradiente de prótons através da membrana mitocondrial interna.
Os mediadores químicos são substâncias endógenas e exógenas que são
QuímicaOs mediadores químicos são substâncias endógenas e exógenas que são liberadas durante o processo de inflamação. São responsáveis por desencadear, amplificar e controlar a reação inflamatória e a resposta imune. As aminas vasoativas, a serotonina e a histamina provocam na resposta imune:
Em uma situação de parada cardíaca, há aumento da produção de ácido
QuímicaEm uma situação de parada cardíaca, há aumento da produção de ácido lático pelas células em hipóxia ou anóxia. Consequentemente, a concentração plasmática de prótons aumenta e o pH sanguíneo diminui. Para manter o equilíbrio ácido-base do organismo depende de sistemas-tampão extracelulares, sendo o principal o do íon bicarbonato, da função respiratória e da função renal. Considerando as informações apresentadas, analise as afirmativas a seguir:
I. O íon bicarbonato reage com o excesso de prótons, formando ácido carbônico que é convertido pela anidrase carbônica em gás carbônico e água. Em seguida, o sistema respiratório elimina o excesso de gás carbônico formado durante a reação química entre o íon bicarbonato e próton.
II. Para compensar a acidose metabólica causada pela parada cardíaca, o paciente apresentará hiperventilação para reduzir a pressão parcial de gás carbônico no sangue.
III. Os rins contribuem para neutralizar o excesso de prótons no plasma por meio da síntese de novos íons bicarbonato e aumento da excreção de prótons pelos néfrons.
IV. A administração intravenosa de bicarbonato de sódio no paciente vai disponibilizar mais íons bicarbonato para neutralizar o excesso de prótons liberados pelo ácido lático.
Os carboidratos obtidos da alimentação, como amido, glicogênio
QuímicaOs carboidratos obtidos da alimentação, como amido, glicogênio, celulose, lactose e sacarose, precisam ter as suas ligações glicosídicas hidrolisadas, em reações catalisadas por glicosidases específicas presentes na boca e no duodeno. A digestão dos carboidratos maiores é necessária, pois apenas os monossacarídeos, as unidades constituintes desses carboidratos, são absorvidos pela mucosa duodenal.
De acordo com as informações apresentadas na tabela a seguir, faça a associação das definições na Coluna A com seus respectivos conceitos, apresentados na Coluna B.
COLUNA A
I. Enzima presente na mucosa duodenal que degrada um dissacarídeo formado pela frutose e glicose.
II. Possui ligações do tipo beta 1->4 entre os monossacarídeos, o que impede a sua hidrólise nos humanos.
III. Produto formado após a digestão pela enzima alfa-amilase pancreática no duodeno.
IV. Intolerância à lactose se caracteriza pela menor ou ausência da atividade de uma glicosidase.
COLUNA B
1. Maltose
2. Celulose.
3. Lactase.
4. Sacarase.
Certa massa de gás hidrogênio (h2) ocupa um volume de 0,760 l sob
QuímicaCerta massa de gás hidrogênio (h2) ocupa um volume de 0,760 l sob pressão de 125 mm hg, numa dada temperatura. qual o volume ocupado pela mesma massa de h2, na mesma temperatura, sob pressão de 0,100 atm
O que são mediadores químicos? Escolha uma: a. Substâncias químicas
QuímicaO que são mediadores químicos?
Existem substâncias endógenas e exógenas que são liberadas durante
QuímicaExistem substâncias endógenas e exógenas que são liberadas durante o processo de inflamação e são responsáveis por desencadear, amplificar e controlar a reação inflamatória e a resposta imune.
O deslizamento dos filamentos de actina sobre os de miosina acontece
QuímicaO deslizamento dos filamentos de actina sobre os de miosina acontece graças à existência de pontos de união entre esses dois filamentos e, para que ele aconteça, há a necessidade de grande quantidade de:
A atividade enzimática pode ser interrompida ou reduzida pela ação
BASA atividade enzimática pode ser interrompida ou reduzida pela ação de substâncias chamadas de inibidores. Esses inibidores interagem com as enzimas, alterando os parâmetros da cinética química, como a velocidade máxima da reação química e a constante de Michaelis. Os inibidores são importantes para a regulação de vias metabólicas, como também na prática clínica, pois muitos fármacos e substâncias tóxicas atuam na inibição de enzimas. A inibição da enzima pode ser reversível ou irreversível. Os tipos mais comuns de inibição reversível são a competitiva e a não competitiva.
Tomando como referência os inibidores enzimáticos, julgue as afirmativas a seguir em (V) Verdadeiras ou (F) Falsas.
( ) Na inibição competitiva, o valor da constante de Michaelis é aumentado, pois para alcançar a metade da velocidade máxima da reação química, é necessária uma quantidade maior de substrato para competir com os inibidores competitivos pelos sítios catalíticos.
( ) Os inibidores não competitivos, por não competirem pelos mesmos sítios de ligação dos substratos, reduzem o valor da constante de Michaelis. Portanto, esses inibidores sempre aumentam a afinidade da enzima pelo substrato.
( ) Com o aumento da concentração de substratos, é possível anular a inibição competitiva. Na inibição não competitiva, esse efeito não ocorre. Por isso, na inibição não competitiva, não há alteração do valor da constante de Michaelis.
( ) O ácido acetilsalicílico é um inibidor irreversível da enzima ciclo-oxigenase (COX), cujo substrato é o ácido araquidônico. Se aumentarmos a concentração de ácido araquidônico, é possível deslocar o ácido acetilsalicílico do sítio catalítico da COX.
O ciclo do ácido cítrico ou ciclo de Krebs é o conjunto de reações
QuímicaO ciclo do ácido cítrico ou ciclo de Krebs é o conjunto de reações químicas, presente nas mitocôndrias, que corresponde à última etapa oxidativa das fontes energéticas. Portanto, é a via final para onde convergem as vias metabólicas dessas fontes energéticas, transformando os seus esqueletos carbônicos em moléculas de gás carbônico e energia.
Considerando o contexto apresentado pelo texto, analise as seguintes afirmativas:
I. A beta-oxidação é a via metabólica oxidativa dos corpos cetônicos, resultando na formação de moléculas de acetil-CoA. Em seguida, o acetil-CoA entra no ciclo do ácido cítrico.
II. Inicialmente, a glicose é convertida em piruvato pela glicólise. Em seguida, o piruvato é oxidado à acetil-CoA na mitocôndria que, por sua vez, entra no ciclo do ácido cítrico.
III. A remoção do grupo amino dos aminoácidos resulta na formação de cetoácidos, muitos dos quais são intermediários do ciclo do ácido cítrico.
Os lipídeos biológicos são um grupo de compostos quimicamente diversos
BASOs lipídeos biológicos são um grupo de compostos quimicamente diversos, cuja característica em comum que os define é a insolubilidade em água. As funções biológicas dos lipídeos são tão diversas quanto a sua química. Gorduras e óleos são as principais formas de armazenamento de energia em muitos organismos. Os fosfolipídeos e os esteróis são os principais elementos estruturais das membranas biológicas. Outros lipídeos, embora presentes em quantidade relativamente pequenas, desempenham papéis cruciais como cofatores enzimáticos, transportadores de elétrons, pigmentos fotossensíveis e outros.
De acordo com as informações apresentadas na tabela a seguir, faça a associação das definições na Coluna A com seus respectivos tipos de lipídeos, apresentados na Coluna B.
COLUNA A
COLUNA B
I. Lipídeo constituído por 3 cadeias de ácidos graxos ligadas a uma molécula de glicerol. Está presente no citoplasma dos adipócitos e atua como reserva energética.
1. Esfingolipídeo
II. Lipídeo constituído por 2 cadeias de ácidos graxos e um grupo cabeça polar ligados a uma molécula de glicerol. Componente estrutural da membrana plasmática.
2. Triacilglicerol
III. Lipídeo constituído por 2 cadeias de ácidos graxos e um grupo cabeça polar ligados à esfingosina. Componente estrutural da membrana plasmática.
3. Glicerofosfolipídeo
IV. Lipídeo constituído por um núcleo esteroide, que consiste em 4 anéis carbônicos fundidos. Responsável em dar estabilidade à membrana plasmática e precursor de produtos biológicos.
4. Colesterol
O metabolismo dos aminoácidos resulta na formação de amônia que
QuímicaO metabolismo dos aminoácidos resulta na formação de amônia que, via circulação sanguínea, é transportada para o fígado. Neste órgão, a amônia, um composto muito tóxico, é convertida em ureia, um composto menos tóxico e facilmente excretado pela urina, por um conjunto de reações químicas mitocondriais e citosólicas. Com relação às informações do texto e seus conhecimentos, analise o excerto a seguir, completando as lacunas. A presença de grupo amino impede o metabolismo oxidativo do aminoácido para a produção de energia. Por isso, o grupo amino é removido dos aminoácidos, em uma reação catalisada pela ____________, para formação do ____________ que, em seguida, com a adição de mais uma amônia, é convertido em ____________. Nos músculos esqueléticos, o grupo amino dos aminoácidos é transferido para o piruvato, resultando na formação de ____________. Esses dois aminoácidos transportam a amônia para o fígado. ____________ é o conjunto das reações químicas que convertem amônia em ureia nos hepatócitos.
Os triacilgliceróis são reservas energéticas fundamentais para
QuímicaOs triacilgliceróis são reservas energéticas fundamentais para os animais e estão armazenados no tecido adiposo, enquanto os fosfolipídeos, componentes da membrana plasmática, desempenham papéis na interação e sinalização celulares. Finalmente, o colesterol, o esterol presente nos animais, importante para a estabilidade da membrana plasmática, além de ser precursor de vários produtos biológicos, como os sais biliares, as vitaminas lipossolúveis e os hormônios esteroides.
Com relação às informações do texto, analise o excerto a seguir, completando as lacunas.
O triacilglicerol, também chamado de triglicéride ou gordura neutra, é composto por três moléculas de ____________ ligadas a uma molécula de ____________. Os fosfolipídeos possuem estruturas mais variadas, mas em comum apresentam natureza anfipática, com uma porção ____________ constituída por ácidos graxos e uma ____________ constituída por diferentes grupos químicos. O colesterol, por sua vez, é constituído por um núcleo ____________.
Os aldeídos possuem em um dos substituintes um hidrocarboneto
QuímicaOs aldeídos possuem em um dos substituintes um hidrocarboneto (alcano, alceno, alcino ou aromático) e em outro um hidrogênio. Já as cetonas possuem dois grupos hidrocarbonetos. Os ácidos carboxílicos possui um hidrocarboneto como e uma hidroxila (OH) como . Substituir esta hidroxila leva a inúmeras outras funções, como os ésteres (), ou anidridos de ácido (). Quando no lugar da hidroxila temos um átomo de cloro você terá um cloreto de ácido (ou cloreto de acila), já o nitrogênio (, ou ) leva à amidas.
Nas células beta-pancreáticas, GLUT-2 atua como um sensor de glicemia
QuímicaNas células beta-pancreáticas, GLUT-2 atua como um sensor de glicemia para a liberação de insulina. Logo após as refeições, quando há hiperglicemia, GLUT-2 permite a entrada de quantidade significativa de glicose nas células beta-pancreáticas. Com isso, aumenta a taxa de oxidação de glicose, o que resulta em maior produção de energia, armazenada nas moléculas ATP. Em seguida, ocorre uma série de eventos, como podemos ver na figura seguinte, que leva à liberação de insulina pelas células beta-pancreáticas.
Considerando o contexto apresentado pelo texto e pela figura, analise as seguintes afirmativas:
I. GLUT-2 tem grande afinidade pela glicose, por isso, durante a hipoglicemia, há entrada de grande quantidade de glicose nas células beta-pancreáticas. Parte considerável dessa glicose será utilizada para produzir ATP, o que inibirá a secreção de insulina.
II. O aumento da concentração intracelular de ATP promove o bloqueio dos canais de potássio sensíveis ao ATP, o que impede o efluxo de íon potássio das células. A consequência é o acúmulo desses íons na célula beta-pancreática, o que leva à despolarização.
III. Os íons cálcio são fundamentais para a exocitose das moléculas de insulina. O influxo desses íons só é possível com a despolarização da célula beta-pancreática, o que ativa os canais cálcio-voltagem-dependentes.
IV. GLUT-2 pancreático atua como sensor de glicemia, pois essa isoforma da GLUT tem baixa afinidade pela glicose. Portanto, GLUT-2 só capta glicose em quantidade significativa em situação de hiperglicemia, por isso, atua como sensor que detecta hiperglicemia e que permite a liberação de insulina.
O glicogênio é a reserva de glicose das células animais, sendo que
QuímicaO glicogênio é a reserva de glicose das células animais, sendo que os hepatócitos e as fibras musculares esqueléticas possuem as maiores concentrações intracelulares de glicogênio. Quando ocorre a glicogenólise, são liberadas unidades de glicose-6-fosfato, que não possuem afinidade por GLUT e, portanto, não saem das células. A enzima glicose 6-fosfatase é responsável em catalisar a clivagem do fosfato da glicose-6-fosfato, o que resulta na formação da glicose livre, que interage com GLUT e consegue sair da célula.
Com relação às informações do texto, analise o excerto a seguir, completando as lacunas.
Nas células ____________, o glicogênio fornece as moléculas de glicose para a via glicolítica para a produção de energia, visto que essas células consomem muita energia. As células ____________ são as únicas que possuem a enzima ____________ que permite a liberação de glicose para a corrente sanguínea. Em casos de doenças ____________, a capacidade desse tecido em liberar glicose durante o jejum e período entre refeições fica prejudicada, o que resulta em ____________.
Após a absorção pela mucosa duodenal, a glicose está presente
QuímicaApós a absorção pela mucosa duodenal, a glicose está presente na circulação sanguínea e precisa entrar nas células para reserva e produção de energia, além de atuar como substrato de outras vias metabólicas, como a vida pentose-fosfato. O problema é que a glicose é uma molécula apolar e, portanto, não consegue atravessar a barreira lipídica da membrana plasmática Então, para entrar na célula, a glicose necessita do auxílio de uma familia de proteínas transmembranas, chamadas de transportadores de glicose (GLUT) Muitas isoformas de GLUT já foram identificadas, com propriedades funcionais diferentes.
Considerando o contexto apresentado pelo texto, analise as seguintes afirmativas:
I. A Isoforma GLUT-2 hepática só é ativada em situação de hiperglicemia, como após as refeições. Em resposta, os hepatocitos secretam Insulina, um hormónio hipoglicemiante.
II. Nos adipocitos e fibras musculares, temos a isoforma GLUT-4, a única dependente da insulina, que permite a captação de glicose por essas células
III. GLUT-2 é a isoforma encontrada nos hepatocitos e células beta-pancreáticas. Essa isoforma tem baixa afinidade pela glicose e so e ativada na hiperglicemia,
Uma das importantes propriedades da água é a capacidade de dissolver
QuímicaUma das importantes propriedades da água é a capacidade de dissolver outras substâncias. A água é considerada solvente universal, porque é muito abundante na Terra e é capaz de dissolver grande parte das substancias conhecidas. Observe a figura e complete as lacunas.
Complete as lacunas a seguir:
As moléculas de água se associam por meio de ligações ____________ descrevendo comportamento geométrico de uma estrutura ______________ com baixo peso molecular, pequeno volume, alto momento dipolar e _______________ constante dielétrica, essas características são responsáveis pelas propriedades especiais da molécula de água como solvente.
Joaquim é um senhor de 65 anos que faz uso de fármacos antidepressivos
QuímicaJoaquim é um senhor de 65 anos que faz uso de fármacos antidepressivos há alguns anos. Nesta semana que passou, Joaquim procurou um outro psiquiatra em uma cidade vizinha, que sugeriu que ele começasse gradualmente a diminuir a quantidade de fármacos antidepressivos substituindo-os por um programa de atividade física sob a supervisão de um profissional responsável, pois o exercício físico libera a mesma substância que está presente nos fármacos antidepressivos.
As moléculas de ácido graxo em um composto lipídico interagem entre
QuímicaAs moléculas de ácido graxo em um composto lipídico interagem entre si por meio de interações intermoleculares apolares. A presença de ligações duplas entre os carbonos da cadeia de ácido graxo interfere no número de interações intermoleculares entre os ácidos graxos. Assim, dependendo do predomínio do tipo de ácido graxo, saturado ou insaturado, o composto lipídico pode se apresentar como sólido ou líquido, na temperatura ambiente.
Considerando o contexto apresentado pelo texto, analise as seguintes afirmativas:
I. Os ácidos graxos saturados possuem cadeia hidrocarbônica estendida, o que permite o máximo de interações entre essas moléculas.
II. Os ácidos graxos, sendo moléculas apolares, interagem entre si por meio de ligações de van der Waals, ligações fracas e momentâneas.
III. Os pontos de fusão dos ácidos graxos aumentam na presença de ligações duplas nas cadeias hidrocarbônicas.
Células fotossensíveis são aquelas que recebem luz e constituem uma
QuímicaCélulas fotossensíveis são aquelas que recebem luz e constituem uma camada profunda formada por “cones e bastonetes”. Dessa forma:
I. Os bastonetes se adaptam à visão com pouca luz, já os cones se ajustam para a visão com luz de maior intensidade e, ainda, para a visão de cores.
II. Normalmente, o número de células bastonetes é muito menor que o número de cones, sendo que nas regiões periféricas predominam os bastonetes.
III. O número de cones diminui progressivamente até a região da mácula densa, e na região central só existem cones.
IV. Na região periférica da retina, os bastonetes ligam-se às células ganglionares.
V. Para os cones, existem conexões com fibras do nervo óptico.